摘要
癌症免疫治療中目前最熱門的為免疫檢查點抑制劑 (immune checkpoint inhibitors),它主要包含了三大類的藥品:anti-cytotoxic T-lymphocyte antigen 4(anti-CTLA-4),anti-programmed cell death 1(anti-PD-1) 及 anti-programmed cell death ligand 1(anti-PD-L1),臨床試驗皆證實比傳統治療上有較好的治療效果,可以延長病人的壽命,但是伴隨著使用此類藥品的病人數增加,越來越多的毒性被報導出來,尤其是因為此類藥品刺激自體免疫來對抗癌細胞,而自體免疫的活性過高,反而會影響到全身的器官造成發炎,目前比較常見的免疫相關副作用有皮膚、內分泌、肝臟、腸胃道及肺臟方面,針對這些不良反應我們綜整出目前的處置方式及考量點,供臨床上使用及注意。期望免疫檢查點抑制劑能更有效及安全的用於癌症病人。
關鍵字:免疫檢查點抑制劑、免疫相關的副作用、Immune checkpoint inhibitors、Immune-related adverse events
壹、前言
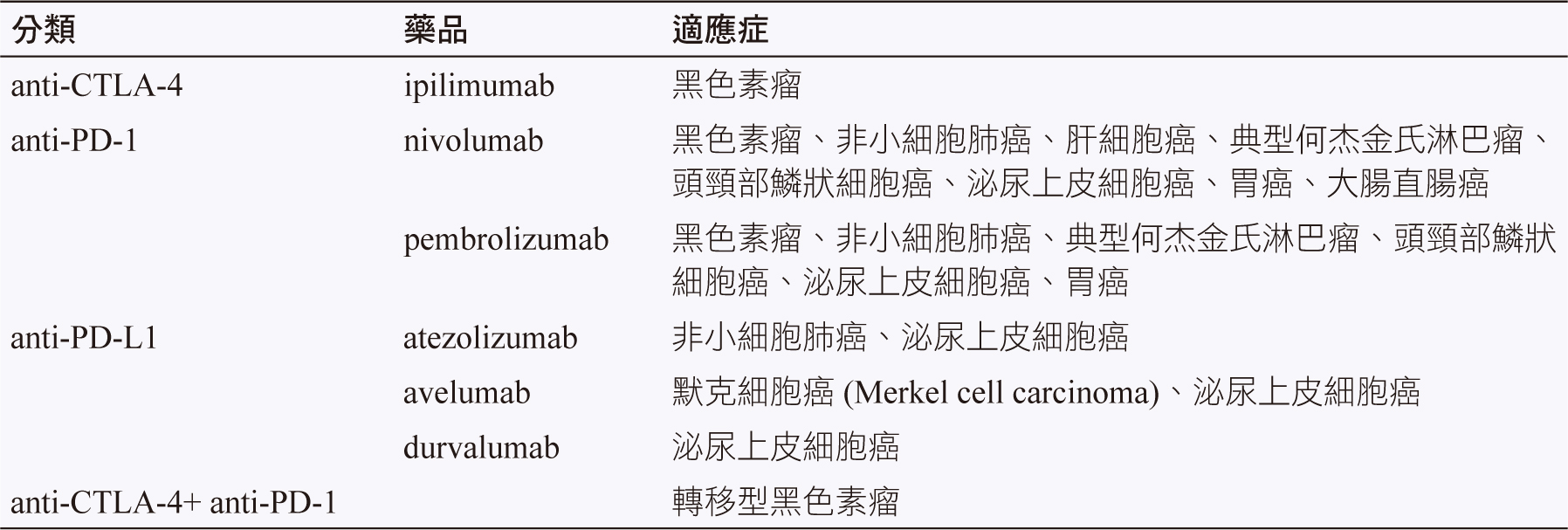
癌症一直都是讓人聞之喪膽的疾病,在醫療進步下,自傳統的化療藥演變至標靶治療,目前最新的藥品是免疫檢查點抑制劑,藉由刺激人體自身免疫系統來攻擊癌細胞,達到抗癌的效果。目前臨床上使用的藥品有3大類,分別是 anti-CTLA-4,anti-PD-1及 anti-PD-L1,共有藥品6項 (表一),本篇以整理歐洲腫瘤學會指引 (European Society for Medical Oncology Guideline, ESMO) 及美國國家癌症資訊網指引 (National Comprehensive Cancer Network Guideline, NCCN),針對免疫檢查點抑制劑的作用機轉及免疫相關副作用的內容,提供給臨床使用者做為參考。
表一 免疫檢查點抑制劑藥品1
貳、免疫檢查點抑制劑作用機轉
人類的T細胞在1991年被發現有辨識腫瘤細胞的能力2,其辨識方式為藉由T細胞接受器與抗原呈現細胞 (antigen presenting cell, APC) 上的主要組織相容性複合體 (major histocompatibility complex, MHC) 結合,活化細胞毒性T淋巴球細胞 (cytotoxic T lymphocyte) 使腫瘤細胞溶解與凋亡,但是T細胞與抗原呈現細胞的結合力沒有B細胞強,所以需要共同刺激分子 (co-stimulatory molecule) 加強其結合力,這些共同刺激分子像是 CD28、B7,當抗原呈現細胞上 B7與T細胞的 CD28結合會刺激樹突細胞分泌白細胞介素6 (interleukin-6, IL-6),然後負調控 (downregulate) 干擾素γ,找有 PD-L1的細胞攻擊,不過 B7比較傾向與T細胞的 CTLA-4結合,而不是 CD28,當 B7與T細胞的 CTLA-4結合反而會抑制T細胞活化,不會產生胞殺性作用 (cytotoxic single),同樣的腫瘤細胞想要生存會產生 PD-L1,PD-L1與T細胞的 PD-1結合一樣會抑制T細胞活化3,4,所以免疫檢查點抑制劑就是針對 CTLA-4、PD-1及 PD-L1做阻斷,達到T細胞持續活化之功能。
參、 免疫檢查點抑制劑引起免疫相關的副作用
影響的器官很多,可能的原因不明,主要與T細胞、抗體 (antibody) 及細胞激素 (cytokine) 有關,目前發現心肌炎 (myocarditis) 的心肌細胞有T細胞浸潤,可能是T細胞攻擊到正常細胞;抗甲狀腺抗體持續釋放攻擊甲狀腺造成發炎;細胞激素在腸道濃度提高造成腸道炎1;而動物研究發現腦下垂體有單核球浸潤,使抗腦下垂體的抗體啟動補體系統造成其發炎。
免疫相關的副作用在用藥後數週至數月間會發生,文獻指出約3.6週會開始出現皮膚的副作用,像是紅疹、搔癢等,約5週後會出現腹瀉的情況,用藥6週後才會出現肝臟及腦下垂體的毒性5,且同時併用兩種免疫檢查點抑制劑會提前副作用發生的時間,甚至停藥後1年還有可能會出現。
副作用發生機率以各類藥品來看,anti-CTLA-4較 anti-PD-1易發生嚴重的副作用,ipilimumab 3 mg/kg 發生率為60%-85%,以輕微的副作用居多,高劑量下 (ipilimumab 10 mg/kg) 也會提高副作用發生率,nivolumab 發生率為74%-85%,pembrolizumab 發生率則為輕微的副作用是57%-60%,嚴重的副作用是14%5。
以下針對臨床上比較常見的副作用逐一做說明:
一、皮膚紅疹、搔癢
是免疫檢查點抑制劑使用後最早發生的副作用,通常給藥後數週內發生,發生機率高,在 ipilimumab 的發生率為43%-45%,在 anti-PD-1發生率為34%,不過這些數據可能有被低估,因為這些病人在用藥後並沒有定期給皮膚科醫師追蹤檢查,嚴重度會依照常見不良事件評量標準 (Common Terminology Criteria for Adverse Events, CTCAE) 分級,以皮膚異常來說,第1級 (grade 1, G1) 為紅、腫、熱、痛的異常範圍佔體表面積的10%以下,第2級 (grade 2, G2) 為體表面積的10%-30%,第3級 (grade 3, G3) 為體表面積的30%以上,第4級 (grade 4, G4) 有危及生命需要住進加護病房治療,像是史蒂芬強森症候群 (Steven-Johnson Syndrome, SJS) 及毒性表皮溶解症 (Toxic Epidermal Necrolysis, TEN),處置方式主要是使用外用的類固醇藥膏及抗組織胺藥品 (表二),搔癢症狀嚴重的話,可以考慮使用 prednisolone 0.5-1 mg/kg/day、GABA agonists、aprepitant 及 omalizumab 進行治療。
表二 紅疹的處置方式5,6
(一)甲狀腺功能異常
較常見於anti-PD-1,發生率約5%-10%,甲狀腺功能低下 (hypothyroidism) 較甲狀腺功能亢進症 (hyperthyroidism) 來的常見,甲狀腺功能低下依 NCCN 建議可以繼續使用免疫檢查點抑制劑,但須持續監測甲狀腺功能 (thyroid function test, TFT),必要時可考慮使用 levothyroxine 0.5-1.5 μg/kg,而針對老年人則建議以低劑量開始給予。目前之指引並未將甲狀腺功能異常明確分級,臨床上可參考美國臨床腫瘤學 (American Society of Clinical Oncology, ASCO) 以促甲狀腺激素 (Thyroid-stimulating hormone, TSH) 之檢驗值分級,G1為 TSH 4-10 mU/L,G2為 TSH > 10 mU/L,G3及 G4則表示為更嚴重的狀況7。
甲狀腺毒性風暴 (thyrotoxicosis),其處理方式為可以繼續使用免疫檢查點抑制劑,有症狀則使用 propranolol 10-20 mg Q4-6H 或 atenolol 或 metoprolol 直到症狀緩解,於4到6週內重複檢驗甲狀腺數值,若抗促甲狀腺激素抗體 (anti-TSH receptor antibody) 為陽性,考慮使用 carbimazole,有疼痛的狀況下可以考慮使用 prednisolone 0.5 mg/kg,若未緩解使用I-123 檢測是否為甲狀腺功能亢進症及格里夫氏症 (Graves' disease),TSH >10 mU/L 則開始使用 levothyroxine,若以上方式皆無法控制,建議暫停免疫檢查點抑制劑。
(二)垂體炎 (hypophysitis)
垂體炎較常發生在 anti-CTLA-4藥品上,發生率為1%-16%,若出現頭痛及視力模糊的症狀要立即做鑑別診斷,確認是否為腫瘤轉移至腦部或是因免疫引起的垂體炎,在腦部的核磁共振攝影下會發現腦下垂體有腫脹及變大的情況,血液方面的數值會出現促甲狀腺激素、促腎上腺皮質激素 (adrenocorticotropic hormone, ACTH)、促卵泡激素 (follicle-stimulating hormone, FSH) 及促黃體生成素 (luteinizing hormone, LH) 均偏低。
建議處理為暫停使用免疫檢查點抑制劑,嚴重的狀況下,像是頭痛、噁心、嘔吐、發燒等,使用 methylprednisolone 1-2 mg/kg 直到症狀緩解,還有可考慮使用賀爾蒙補充 (hormone replacement),需每天早上10點使用口服 hydrocortisone 20 mg,下午口服 hydrocortisone 10 mg。
三、肝功能異常
建議所有的病人在使用免疫檢查點抑制劑前,先測肝功能,肝功能異常在各類藥品間發生率差不多,約5%-10%,通常在適當的治療後4到6週就會恢復至正常,如果沒有則評估是否有其他藥品影響肝功能,像是中草藥,或是巨細胞病毒 (cytomegalovirus) 感染。肝功能的嚴重程度分級是依 ALT/AST 數值,G1為小於3倍正常值,G2為3-5倍正常值,G3為5-20倍正常值,G4則是大於20倍正常值。當嚴重程度大於 G2時,則停止使用免疫檢查點抑制劑,持續監測轉胺酶 (transaminases)、膽紅素 (bilirubin)、國際標準化比值 (international normalized ratio, INR) 及白蛋白 (albumin),若肝功能變差則使用口服 prednisolone 0.5-1 mg/kg/day,若未改善則加重 prednisolone 劑量至1-2 mg/kg/day,甚至改用針劑 (methyl) prednisolone 2 mg/kg,三天後症狀未改善則考慮 mycophenolate (MMF) 0.5-1g Q12H,使用 MMF 後狀況未改善,加上 tacrolimus。
四、腹瀉、腸炎
幾乎三分之一的病人會產生腹瀉的症狀,尤其是以 anti-CTLA-4的使用者產生腸炎居多,若正好同時併用非類固醇消炎止痛藥 (Non-Steroidal Anti-Inflammatory Drug, NSAID) 也會增加 anti-CTLA-4引起腸炎的風險,發生時間在使用 anti-CTLA-4第1次至第10次給藥間都有可能出現,即使在藥品完全代謝清除後。可能出現的症狀有腹痛、血便、體重下降、發燒及嘔吐,血液方面會有貧血、C-反應蛋白 (C-reactive protein) 升高、白蛋白下降,糞便中會出現糞便鈣衛蛋白 (calprotectin),可以藉由腸鏡檢查或切片確診5。
嚴重度分類方式與腹瀉次數有關,G1為一天腹瀉少於4次,G2為腹瀉4到6次,G3為7次以上,G4為危及生命。G1處理方式為使用 loperamide 4 mg 一劑,然後12小時內每餐30分鐘前給予2 mg,直到沒有腹瀉 (最大量為16 mg/day),飲食方面要避免食用高纖及乳糖,若G1持續大於14天或是G2大於3天,則使用非腸溶性的 prednisolone 0.5-1mg/kg 或口服 budesonide 9 mg,NCCN 建議及早使用針劑 methylprednisolone 1 mg/kg/day,若2至3天沒有改善則考慮 infliximab,若使用 infliximab 後復發則考慮 vedolizumab8,同時也可併用 MMF 0.5-1g BID 或是 tacrolimus。
五、肺炎
好發於肺功能不佳者,像是吸菸者,以 anti-PD-1/ anti-PD-L1發生率較高,86%的病人會在停止使用免疫檢查點抑制劑及使用免疫抑制劑 (immunosuppression) 後好轉,發生時間為給藥後9天至19.2個月。
嚴重度分級依肺部異常的面積百分比來分,G1為佔肺部的25%,G2為25%-50%,G3為50%以上,G4為插管或氣切。
無論肺炎的嚴重度,只要有發生則暫停免疫檢查點抑制劑,每2至3天觀察一次症狀,且考慮使用經驗性抗生素 (empiric antibiotics),若沒有感染或是使用抗生素48小時後沒有改善,則加上口服 prednisolone 1-2 mg/kg/day。G3/G4或是 G2症狀大於2至3天,使用針劑 (methyl)prednisolone 2-4 mg/kg,若兩天內沒有改善,則考慮 infliximab 5 mg/kg 或是有發生肝毒性就改用 MMF 1-1.5 g BID,因為 infliximab 本身具有肝毒性的副作用,甚至考慮使用 IVIG (intravenous immunoglobulin) 0.4 mg/kg 連續施打5天。
六、臨床考量
目前對於免疫檢查點抑制劑引起免疫相關的副作用還有很多討論,像是使用免疫抑制劑治療會不會影響之前的抗腫瘤效果,回溯性研究資料顯示是沒有差異的1,但需注意使用類固醇可能會引起的副作用,像是血糖升高、水牛肩、月亮臉以及焦慮等。另外,要注意可能增加病人得到伺機性感染的風險9,根據一個大型的研究發現有13.5%的病人出現嚴重的感染,所以建議使用 prednisolone 每天劑量20 mg 大於4週者,投藥預防肺囊蟲肺炎 (pneumocystis jirovecii prophylaxis) 發生。
至於適不適合再次使用免疫檢查點抑制劑,則依免疫相關的副作用嚴重度而定,若是出現嚴重的心臟、肺臟、神經方面的毒性,則不建議再次使用。先前使用 anti-CTLA-4產生副作用的病人,可以考慮改用 anti-PD-1,有文獻提及觀察38位病人再次使用免疫檢查點抑制劑,其中19位病人沒有產生副作用,10位產生新的副作用,9位復發,但嚴重度較先前為低1。
病人本身的肝、腎功能及年齡並不會對免疫相關副作用的發生率造成影響,另外,有研究顯示肌少症 (sarcopenia) 病人可能會比較容易產生免疫相關副作用,但也有可能是病人本身營養不良所致10。若本身有自體免疫的疾病或是愛滋病,為避免使本身的疾病惡化,不建議使用免疫檢查點抑制劑。
肆、結論
由於免疫檢查點抑制劑與免疫相關的副作用可能表現於身體的各個器官,牽涉相當廣泛,導致病人可能分散至急診或各醫療專科就診尋求協助,因此有關於此類藥品不良反應正確處置之跨領域訊息傳遞非常重要,本文綜整現有的文獻證據提供臨床照護者參考,期望免疫檢查點抑制劑的使用能更有效及安全的用於癌症病人。
Management of
Immune Checkpoint Inhibitors - associated
Adverse Effect and Clinical Considerations
Chun-Ju Wang, Fang-Ruei Syu, Chi-Lan
Kao, Wan-Tsui Huang
Department of Pharmacy, Cathay General Hospital
Abstract
Immune checkpoint inhibitors (ICIs) are novel treatment options for cancer patients. ICIs include cytotoxic T-lymphocyte antigen 4 (CTLA-4), programmed cell death 1 (PD-1) and programmed cell death ligand 1 (PD-L1). Several clinical trials indicated that ICIs achieved better treatment outcomes than conventional chemotherapy and extended lifespan of the patients. However, notable drug-associated adverse events of collateral damage to major organs due to enhanced immune response, or immune-related adverse events (irAEs), were frequently reported. The commonly seen irAEs affected skin, endocrine, liver, gastrointestinal tract and lungs. In this article, we summarize ICIs-related irAEs, clinical issues and current approach for the management of ICIs-related irAEs.
參考資料:
1. Postow MA, Sidlow R, and Hellmann MD: Immune-Related Adverse Events Associated with Immune Checkpoint Blockade. N Engl J Med 2018; 378: 158-68.
2. Oiseth SJ, Aziz MS: Cancer immunotherapy: a brief review of the history, possibilities, and challenges ahead. J Cancer Metastasis Treat 2017; 3: 250-61.
3. Byrne EH, Fisher DE: Immune and Molecular Correlates in Melanoma Treated With Immune Checkpoint Blockade. Cancer 2017; 123: 2143-53.
4. Wieder T, Eigentler T, Brenner E, et al: Immune checkpoint blockade therapy. J Allergy Clin Immunol 2018. (Unpublished material)
5. Haanen JBAG, Carbonnel F, Robert C, et al: Management of toxicities from immunotherapy: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2017; 28 (Suppl 4): iv 119-42.
6. Management of immunotherapy-Related Toxicity. NCCN Guidelines for supportive care. Version 1. 2018.
7. Postow M, Wolchok J: Toxicities associated with checkpoint inhibitor immunotherapy. UpToDate. Available from: https://www.uptodate.com (cited: 04/17 /2018)
8. Bergqvist V, Hertervig E, Gedeon P, et al: Vedolizumab treatment for immune checkpoint inhibitor-induced enterocolitis. Cancer Immunol Immunother 2017;66:581–92.
9. Weber JS, Postow M, Lao CD, et al: Management of Adverse Events Following Treatment With Anti-Programmed Death-1 Agents. The Oncologist 2016; 21: 123-40.
10. Daly LE , Power DG, O'Reilly A, et al: The impact of body composition parameters on ipilimumab toxicity and survival in patients with metastatic melanoma. British Journal of Cancer 2017; 116: 310-7.
通訊作者:黃婉翠/通訊地址:台北市大安區仁愛路四段 280 號
服務單位:國泰綜合醫院藥劑科藥師/聯絡電話:(O) 02-27082121 ext 3810