摘要
自2011年第一個免疫檢查點抑制劑 (immune checkpoint inhibitors,ICIs) ipilimumab 核准用於治療黑色素細胞瘤,之後陸續有5個 ICIs 上市。目前可使用的 ICIs 包括 CTLA-4抑制劑、PD-1抑制劑、PD-L1抑制劑。ICIs 可治療多種不同的癌症和提供較高比例的長期存活。ICIs 治療腫瘤的反應有可能會出現假性惡化 (pseudo-progression) 之非典型的治療反應模式,因此不要太早判定治療無效。使用 ICIs 引起副作用因而停藥者,其原本的療效仍可持續。併用不同機轉的 ICIs 或是不同策略的免疫治療,或是 ICIs 合併化療、標靶藥物、放射線,可使更多病人獲得治療反應。ICIs 的未來挑戰包括:找到最適當的劑量和藥物組合、給藥順序、治療持續時間、最佳的生物標記可作為預先評估 ICIs 的療效。
關鍵字:免疫檢查點抑制劑、immune checkpoint inhibitor、ipilimumab、nivolumab、pembrolizumab
壹、前言
自2011年第一個免疫檢查點抑制劑 (immune checkpoint inhibitors,ICIs) ipilimumab 核准用於治療黑色素細胞瘤 (melanoma),之後陸續有5個 ICIs 上市,包括 pembrolizumab、nivolumab、atezolizumab、avelumab、durvalumab。其中 ipilimumab 是第四類細胞毒殺T細胞抗原 (cytotoxic T lymphocyte antigen 4,CTLA-4) 抑制劑,pembrolizumab、nivolumab 是第一類程序性細胞死亡蛋白質 (programmed cell death protein 1,PD-1) 抑制劑,atezolizumab、avelumab、durvalumab 是第一類程序性細胞死亡配體 (programmed cell death ligand 1,PD-L1) 抑制劑。本文將說明 ICIs 帶給癌症治療的衝擊,以及未來使用 ICIs 需要突破的瓶頸。
貳、免疫檢查點抑制劑
T淋巴細胞 (T細胞) 上有許多免疫檢查點,有些是促進T細胞活化就像踩油門,有些反而是抑制T細胞就像踩煞車。其中 CTLA-4 和 PD-1是屬於抑制性免疫檢查點,因此研發藥物來抑制 CTLA-4 或 PD-1,也就是拿掉煞車,即可重新喚醒T細胞發揮其抗癌作用,這就是 ipilimumab 和 PD-1 抑制劑的作用機轉。此外,當T細胞靠近癌細胞時,癌細胞時常會出現 PD-L1配體,由於 PD-L1和 PD-1結合後會導致T細胞無法發揮作用,因此研發藥物來抑制 PD-L1配體,則可以恢復T細胞原本功能,這就是 PD-L1抑制劑的作用機轉。
參、臨床效益
不同於傳統的化療和標靶治療,ICIs 有其獨特的臨床效益,現論述如下:
一、可廣泛治療多種癌症
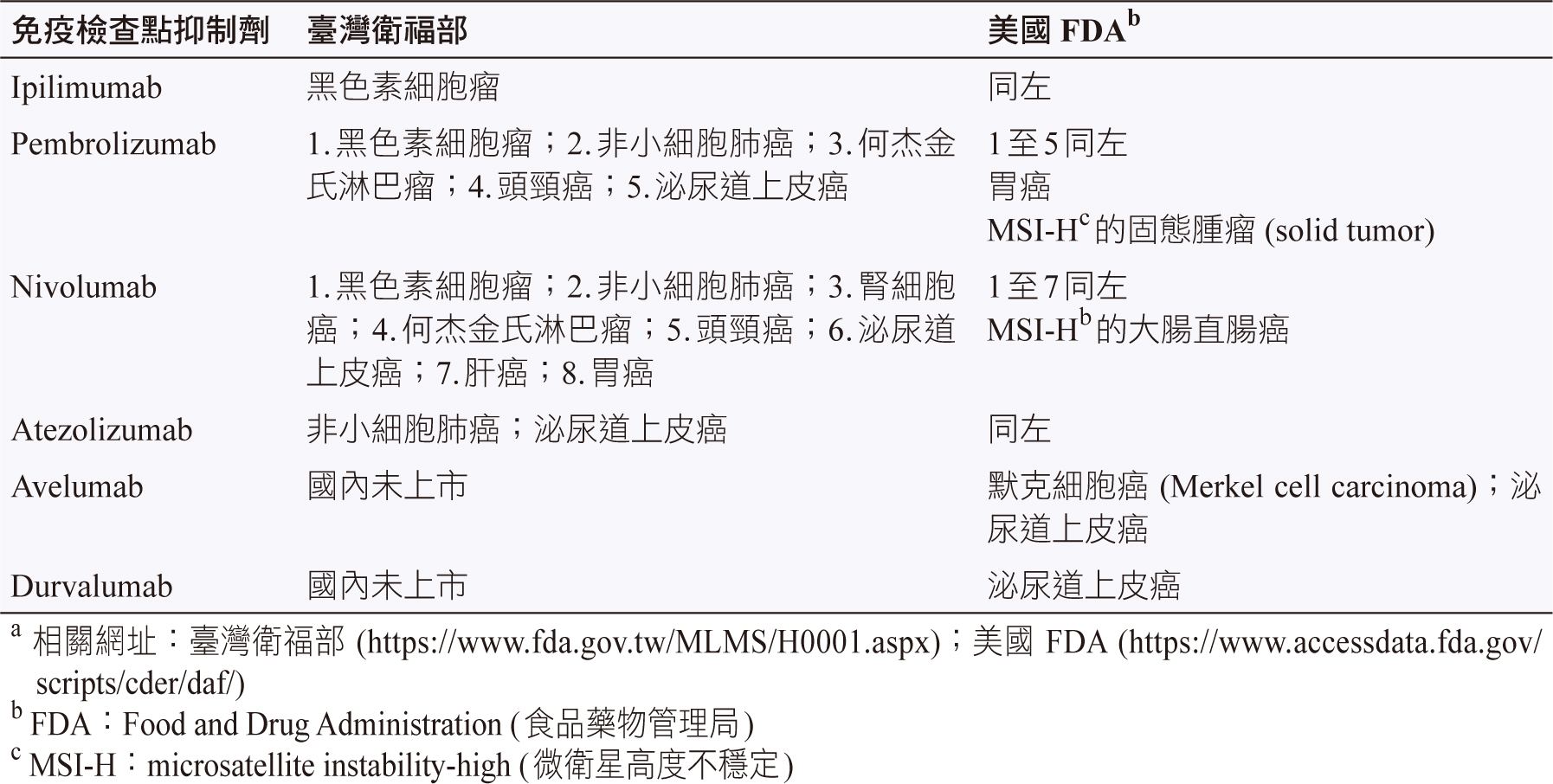
由於 ICIs 作用方式是活化自身的免疫系統去對抗癌症,因此它們可用於治療不同的癌症 (表一)。值得注意的是 pembrolizumab 已取得所有固態腫瘤 (solid tumor) 的適應症,只要其腫瘤呈現微衛星高度不穩定 (microsatellite instability-high,MSI-H)。目前,ICIs 中只有 ipilimumab 獲得臺灣健保給付。
表一 免疫檢查點抑制劑核准的適應症a
二、提供較高比例的長期存活
ICIs 的介入使得更多病人能夠長期存活,以黑色素細胞瘤為例:針對晚期已無法手術切除或轉移性黑色素細胞瘤病人,單獨使用 ipilimumab 作為第一線或第二線治療的10年存活率為21%1,而化療和生物化療 (biochemotherapy) 治療轉移性黑色素細胞瘤的10年存活率則小於10%2。又最近資料顯示,比較第一線給予 ipilimumab、nivolumab、ipilimumab 併用 nivolumab 治療晚期黑色素細胞瘤患者的3年存活率分別為34%、52%、58%3。此外,在許多晚期轉移性癌症 (例如:非小細胞肺癌、頭頸癌、腎細胞癌) 的治療上,相較於化療或是標靶藥物 (例如:腎細胞癌第二線標靶藥物everolimus),ICIs 皆能明顯改善存活率4。
三、非典型的治療反應模式
ICIs 治療腫瘤的反應有可能一開始在影像學上顯示腫瘤變大或是出現新的病變 (lesions),但是在持續使用 ICIs 一段時間後,其腫瘤反而縮小,這個現象稱為假性惡化 (pseudo-progression)。假性惡化的原因是免疫細胞 (主要是淋巴細胞) 滲入腫瘤內部造成,而不是腫瘤生長。由於使用 ICIs 可能發生這種非典型的治療反應模式,因此,只要病人的整體狀況許可,即使影像學上顯示疾病惡化,也應繼續使用 ICIs 至少1個月後再次評估。由於臺灣健保規定每3個月才能作一次電腦斷層以評估治療效果,因此當第一次電腦斷層影像結果顯示疾病惡化時,可視病人情況繼續使用 ICIs,若使用 ICIs 達6個月,第二次的電腦斷層影像結果仍顯示惡化時,方可確定該病人對 ICIs 治療無效。
四、停藥後仍有持續的療效
研究發現,併用 ipilimumab 和 nivolumab 治療黑色素細胞瘤的患者中,因副作用而停藥者,其18個月的存活率為79.5%,而全部病人的存活率為73.2%,兩者並無差別5,顯示使用 ICIs 引起副作用因而停藥者,其原本的療效仍可持續。至於 ICIs 要持續使用多久時間才恰當,目前仍未知,有待未來更多的研究來回答此問題。
五、合併治療有更好的療效
經由 CheckMate-067第三期臨床試驗,單用 ipilimumab 的客觀治療反應率 (objective response rate,ORR) 為19%,單用 nivolumab 為43.7%,而 ipilimumab 併用 nivolumab 則為57.6%6,顯示 ipilimumab 併用 nivolumab 有加成作用;併用不同機轉的 ICIs 可提供更佳療效。
ICIs併用化療藥物、標靶藥物也是可利用的策略。相關研究有:pembrolizumab 併用化療藥物 pemetrexed/carboplatin 或 cisplatin 第一線治療非鱗狀非小細胞肺癌的ORR為55%、1年存活率為69.2%、mPFS 為8.8個月,明顯優於化療組的29%(ORR)、49.4%、4.9個月7,8。對於微衛星穩定 (microsatellite stability, MSS) 大腸直腸癌單用 ICIs 治療均顯示無效,然而將atezolizumab合併標靶藥物 cobimetinib 治療,ORR 可達20%,這是一個突破性進展9。此外,在進行放射線治療時,偶爾會發現,照射範圍之外的腫瘤也會縮小,這個現象稱之為遠端免疫效應 (abscopal effect),其成因乃是放射線治療殺死腫瘤細胞,使得腫瘤抗原釋出以誘導T細胞的活化,引起全身性的免疫反應;因此,我們可藉由 ICIs 併用放射線治療來加強此效應。
肆、安全性
ICIs 引起的免疫相關不良事件 (immune-related adverse events,irAEs) 可遍及全身,其中皮膚出現紅疹、腹瀉、大腸炎、甲狀腺功能異常、腎上腺機能不足、肝炎是常見的副作用,而肺臟、中樞神經系統、心臟血管系統、肌肉骨骼系統、血液系統的副作用則少見10。雖然 irAEs 常發生在前三個月,但要注意的是,在使用 ICIs 期間的任何時間點都有可能發生 irAEs,甚至停藥後也會發生;因此,隨時保持警覺是關鍵,一旦發生 irAEs,要立刻給予類固醇10。
伍、未來挑戰
ICIs 的確為癌症治療帶來新的曙光,但是也隨之而來產生新的問題與挑戰,今說明如下:
一、尋求最適當的劑量
(一)Ipilimumab
目前國內核准單獨使用 ipilimumab 用於治療成人無法切除或轉移性黑色素瘤,仿單建議劑量及用法為3 mg/kg、每3週一次。相關研究包括:將單用 ipilimumab 治療晚期黑色素細胞瘤的4個第二期研究資料整合,總人數498人,使用 ipilimumab 的劑量有0.3 mg/kg、3 mg/kg、10 mg/kg,分析結果發現中位存活期 (median overall survival,mOS) 和 ipilimumab 達到血中穩定狀態時的最低濃度 (steady-state trough concentration,Cminss) 呈現明顯正相關,而和劑量較無相關,由 Kaplan-Meier 存活曲線顯示0.3 mg/kg 和3 mg/kg 幾乎重疊;又 irAEs 的發生也和 Cminss 有關11。然而,在一收納727位轉移性黑色素細胞瘤,比較 ipilimumab 3 mg/kg 和10 mg/kg 的存活期和安全性之第三期研究顯示,10 mg/kg 的 mOS 勝過3 mg/kg (15.7個月 vs. 11.5個月,HR 0.84,P = 0.04),但是10 mg/kg 發生嚴重 irAEs (≥ 第3級) 和因 irAEs 致死的百分比也明顯多於3 mg/kg (33.5% vs. 17.4%;1.1% vs. 0.6%)12。
(二)Nivolumab 和 pembrolizumab
對於各種不同之固態腫瘤 (solid tumor,包括非小細胞肺癌、黑色素細胞瘤、腎細胞癌、大腸直腸癌、前列腺癌) 進行 nivolumab 和 pembrolizumab 的曝露量—反應模式 (exposure-response model) 研究,結果顯示 nivolumab 在0.1-10 mg/kg 的劑量範圍內,抗腫瘤的 ORR 雷同,又在此劑量範圍內,發生藥物不良事件的機率也相近;而 pembrolizumab 在2-10 mg/kg 的劑量範圍內也是如此,但是小於1 mg/kg 則效果有限13。臺灣衛福部核准 nivolumab 的劑量為3 mg/kg,每2週一次;pembrolizumab 的劑量為2 mg/kg,每3週一次。由於前述的曝露量—反應模式研究顯示低劑量 nivolumab 也有相當的療效,因此未來 nivolumab 是否可使用較低劑量 (例如:1 mg/kg 甚至更低),則需要更多研究來證明。
二、尋求最合適的 ICIs 合併治療策略
採取 ICIs 合併治療策略時,有關藥物如何組合、給藥順序、投予劑量、給藥間隔、治療期間多長,希望達到療效最大兼顧毒性最小的結果,這些都是相當的挑戰。舉例來說,ipilimumab 3 mg/kg 併用 nivolumab 1 mg/kg 治療黑色素細胞瘤的 ORR 高達57.6%,但是第3或4級 irAEs 的發生率也高達55%7;然而,ipilimumab 的劑量降為 1 mg/kg 併用 nivolumab 3 mg/kg 治療非小細胞肺癌的 ORR 仍維持在57%,但是第3或4級 irAEs 的發生率則大幅降至20%14。給藥順序也會影響治療效果,研究發現,若先施打 nivolumab 3 mg/kg 六次後再接著給予 ipilimumab 3 mg/kg 四次,其療效和安全性類似 ipilimumab 3 mg/kg併用 nivolumab 1 mg/kg;反之,若先施打 ipilimumab 3 mg/kg 四次後再接著給予 nivolumab 3 mg/kg 六次,其療效和安全性則類似單用 nivolumab 3 mg/kg15。
三、尋求最佳的生物標記 (biomarker)
PD-L1表現的百分比,是目前可被用來評估 PD-1/PD-L1抑制劑之療效的生物標記。然而,PD-L1表現百分比的定義分歧,有些是看腫瘤微環境免疫細胞 (immune cell,IC) 上 PD-L1的表現,有些是看腫瘤細胞 (tumor cell,TC) 上 PD-L1的表現,有些是結合 IC 和 TC 一起看;此外,用來測定 PD-L1的抗體皆不同,判定 PD-L1的臨界點 (cut-off) 也不盡相同,以及 PD-L1本身是呈現動態變化,在在都是臨床上需要解決的問題。因此尋求最佳的生物標記,來預先找出哪些病人會因使用 ICIs 得到最大效益,是將來努力的方向。
陸、結論
ICIs 的問市使得癌症治療邁向一個新紀元。目前可使用的 ICIs 包括 CTLA-4抑制劑、PD-1抑制劑、PD-L1抑制劑。ICIs可治療多種不同的癌症和提供較高比例的長期存活。隨著越來越多人使用 ICIs,其 irAEs 的處理也是醫療人員需要密切注意的地方。併用不同機轉的 ICIs 或是不同策略的免疫治療,或是 ICIs 合併化療、標靶藥物、放射線,使得有更多病人能獲得治療反應,這方面的研究發展正在快速進行中。ICIs 的未來挑戰包括:找到最適當的劑量和藥物組合、給藥順序、治療持續時間、最佳的生物標記可作為預先評估 ICIs 的療效。對某些病人來說,ICIs 已經將癌症從死亡的代名詞轉變成慢性病狀態。冀望未來當更多具有證據力的治療策略出現後,讓更多患者能夠受惠以及達到治癒癌症的終極目標。
Immune Checkpoint Inhibitors: Clinical
Characteristics and Future Challenges
Chi-Yuan Cheng1, Tzu-Cheng Tsai1, Wen-Cheng
Chang2
Department of Pharmacy, Chang Gung Memorial
Hospital, Linkou1
Department of Oncology, Chang Gung Memorial
Hospital, Linkou2
Abstract
Ipilimumab, the first immune checkpoint inhibitors (ICIs ), was approved for the treatment of melanoma in 2011, and five ICIs had been listed successively. Currently, available ICIs include CTLA-4 inhibitors, PD-1 inhibitors, and PD-L1 inhibitors. ICIs could be used to treat a broad range of cancer types and provide higher percentage of long-term survival. ICIs may show the atypical pattern of response as pseudo-progression, so do not confirm treatment failure of ICIs too early. Patients who stop ICIs because of adverse drug events generally maintain responses. ICIs with different mechanisms can be combined, and ICIs can be combined with other cancer immunotherapies, chemotherapy, targeted therapy, and radiation to transform more non-responders to responders. Future challenges for ICIs include the optimal dose and combinations, the order of administration, duration of treatment, and the best biomarker to predict the efficacy of ICIs.
參考資料:
1. Hodi FS, O'Day SJ, McDermott DF, et al: Improved survival with ipilimumab inpatients with metastatic melanoma. N Engl J Med 2010;363:711-23.
2. Bhatia S, Tykodi SS, Thompson JA: Treatment of metastatic melanoma: an overview. Oncology (Williston Park) 2009;23:488-96.
3. Wolchok JD, Chiarion-Sileni V, Gonzalez R, et al: Overall Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N Engl J Med 2017;377:1345-56.
4. Thallinger C, Füreder T, Preusser M, et al: Review of cancer treatment with immune checkpoint inhibitors : Current concepts, expectations, limitations and pitfalls. Wien Klin Wochenschr 2018;130:85-91.
5. Hodi FS, Postow MA, Chesney JA, et al: Overall survival in patients with advanced melanoma (MEL) who discontinued treatment with nivolumab (NIVO) plus ipilimumab (IPI) due to toxicity in a phase II trial (CheckMate 069). J Clin Oncol 2016;34(suppl; abstr 9518).
6. Larkin J, Chiarion-Sileni V, Gonzalez R, et al: Combined nivolumab and ipilimumab or monotherapy in untreated melanoma. N Engl J Med 2015;373:23-34.
7. Langer CJ, Gadgeel SM, Borghaei H, et al: Carboplatin and pemetrexed with or without pembrolizumab for advanced, non-squamous non-small-cell lung cancer: a randomised, phase 2 cohort of the open-label KEYNOTE-021 study. Lancet Oncol 2016;17:1497-508.
8. Gandhi L, Rodríguez-Abreu D, Gadgeel S, et al: Pembrolizumab plus chemotherapy in metastatic non-small-cell lung cancer. N Engl J Med. 2018 Apr 16. doi: 10.1056/NEJMoa1801005. [Epub ahead of print]
9. Bendell JC, Kim TW, Goh BC, et al: Clinical activity and safety of cobimetinib (cobi) and atezolizumab in colorectal cancer (CRC). J Clin Oncol 2016;34 (suppl; abstr 3502).
10. Postow MA, Sidlow R, Hellmann MD: Immune-related adverse events associated with immune checkpoint blockade. N Engl J Med 2018;378:158-68.
11. Feng Y, Roy A, Masson E, et al: Exposure-response relationships of the efficacy and safety of ipilimumab in patients with advanced melanoma. Clin Cancer Res. 2013;19:3977-86.
12. Ascierto PA, Del Vecchio M, Robert C, et al: Overall survival (OS) and safety results from a phase 3 trial of ipilimumab (IPI) at 3 mg/kg vs 10 mg/kg in patients with metastatic melanoma (MEL). Ann Oncol 2016;27(suppl 6):vi379-400.
13. Peter L Bonate, Danny R Howard : Pharmacokinetics in Drug Development. Volume 4, Problems and Challenges in Oncology, 1st ed. Switzerland. Springer Verlag, 2016:250.
14. Hellmann MD, Gettinger SN, Goldman J, et al: CheckMate 012: Safety and efficacy of first-line nivolumab and ipilimumab in advanced non-small cell lung cancer. J Clin Oncol 2016;34(suppl; abstr 3001).
15. Weber JS, Gibney G, Sullivan RJ, et al: Sequential administration of nivolumab and ipilimumab with a planned switch in patients with advanced melanoma (CheckMate 064): an open-label, randomised, phase 2 trial. Lancet Oncol 2016;17:943-55.
通訊作者:鄭吉元/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 2915