摘要
高劑量介白素-2 (interleukin-2, IL-2) 是第一個被核准用於治療轉移性腎細胞癌及黑色素癌的免疫療法,可以使少數病人產生持久的抗癌反應並延長其存活時間,不過高劑量 IL-2可能會產生毛細血管滲漏症候群,導致毛細血管通透性增加,使體液滲漏至血管外的組織間隙,另一方面也造成低血容,影響器官灌流甚至導致死亡。不過這些藥物不良反應是與使用劑量相關、可逆的、可以預期並且也是可以被處理。也因此高劑量 IL-2仍然是一種有效及安全的治療選擇。
關鍵字:IL-2、毛細血管滲漏症候群、免疫療法、interleukin-2、capillary leak syndrome、immunotherapy
壹、前言
高劑量介白素-2 (interleukin-2, IL-2) 為第一個用於癌症治療的免疫療法,早在1993年及1998年 FDA 就核准用於治療轉移性腎細胞癌及惡性黑色素癌1。台灣衛福部亦核准用於這兩種癌症治療,也分別在2001年及2004年取得健保給付,IL-2抗腫瘤作用並非直接毒殺癌細胞,而是造成T細胞、B細胞及自然殺手細胞的增殖與活化,激活人體免疫系統對抗癌症細胞,研究顯示高劑量 IL-2治療轉移性腎細胞癌及惡性黑色素癌,雖然只有少數病人可以達到完全反應 (complete response),不過多數完全反應者可以產生持久抗癌反應 (durable response)2-4,並且在沒有其他治療下持續多年,在一篇收錄409位病人,其中轉移性腎細胞癌227位及惡性黑色素癌182位,完全反應者有33位 (8.1%),其中27名 (82%) 從治療開始39個月至148個月仍持續有反應5,然而高劑量 IL-2可能會造成毛細血管滲漏症候群 (capillary leak syndrome, CLS),造成心臟與肺臟等器官損傷甚至死亡。本文報告一位使用高劑量 IL-2治療腎細胞癌導致毛細血管滲漏症候群的藥物不良反應案例。
貳、案例報告
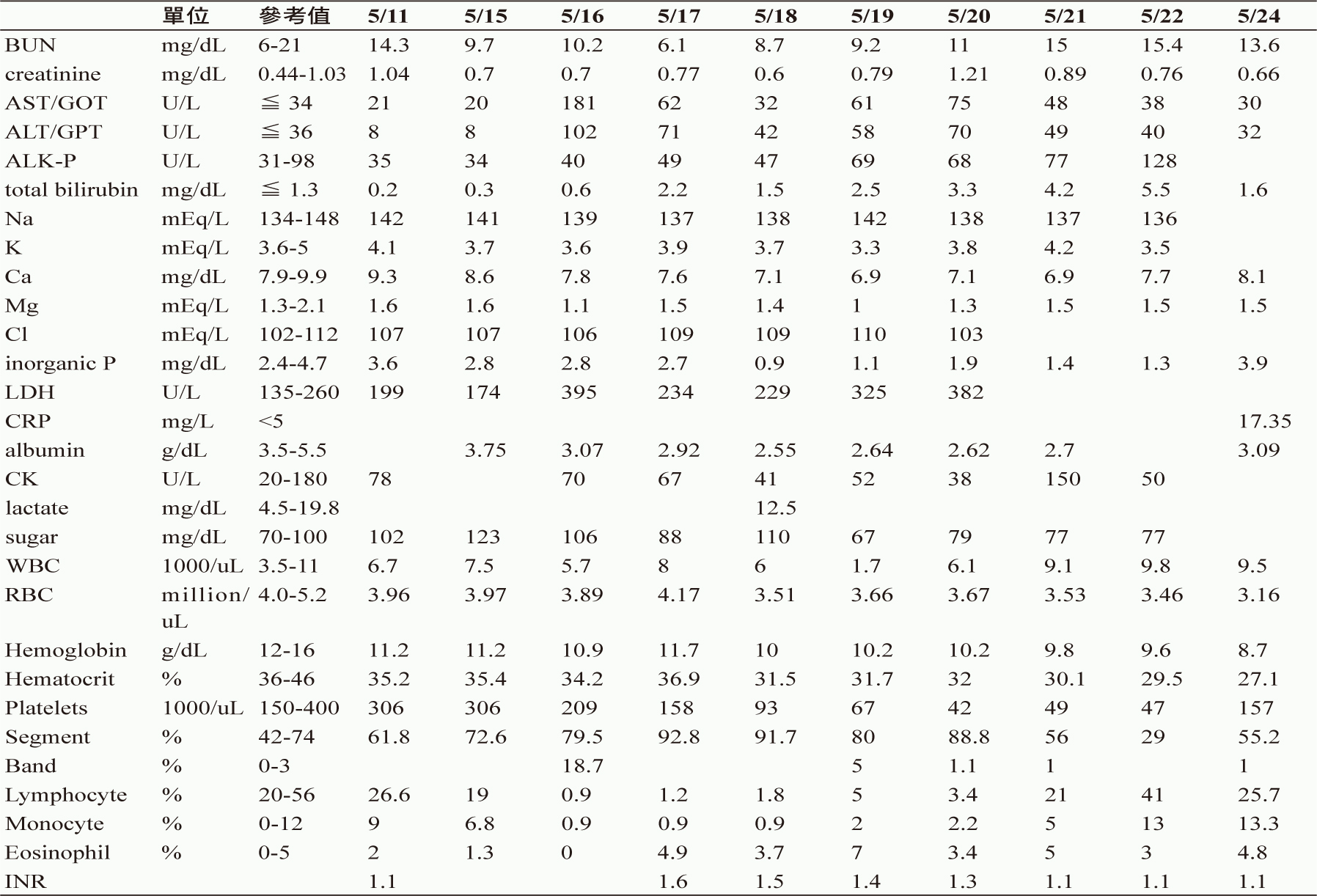
30歲女性病患,身高169公分、體重58公斤,2014年1月診斷右側腎細胞癌,於2014年接受右側根除性全腎切除手術,自2015年起開始接受多種標靶藥物 (sunitinib、pazopanib、everolimus、interferon-α、axitinib、sorafinib) 治療,不過仍治療失敗,經與醫師討論後決定接受高劑量 IL-2治療,治療前安排斷層掃描顯示腦部沒有腫瘤轉移,心電圖檢查為正常竇律,ECOG (Eastern Cooperative Oncology Group, ECOG) 為0分,顯示體能狀態正常,於2018年5月15日轉至加護病房,在當天開始接受第一個劑量治療,於治療前預防性投予 (pre-medication) 包括有 acetaminophen、indomethacin、meperidine、prochlorperazine、loperamide、esomeprazole、diphenhydramine、cefadroxil,病人隔天出現腹痛、發燒、寒顫與低血鎂症等症狀,隨著藥物持續使用出現低血壓、心搏過速、周邊水腫與體重增加,有適時給予輸液補充以改善低血壓,此外病人有焦慮、全身虛弱、低血鉀、低白蛋白血症、臉部及頸部皮膚搔癢、噁心、嘔吐、腹瀉、肝功能異常、寡尿、血液肌酐酸上升、INR (international normalized ratio) 延長、發燒並伴隨有呼吸困難等不適,第四天抽血檢查出現全血球減少症、嗜依紅性白血球增加,最後一天出現發燒、寒顫、肺水腫與呼吸困難,病人意識於治療中皆保持清醒,血壓穩定後給予 furosemide 以改善寡尿、周邊水腫與肺水腫,相關藥物不良反應也在結束治療後逐步改善,不過體重增加近9公斤,5月22日轉至普通病房,三天後出院接受門診追蹤,住院期間相關檢驗報告 (表一)。
表一 病人於治療期間相關生化與血液檢驗報告
參、討論
毛細血管滲漏症候群是 IL-2治療可以預期並且是與使用劑量相關 (dose-dependent) 的藥物不良反應,造成的機轉可能是與 IL-2直接作用在具 CD25表現的內皮細胞 (CD25-expressing endothelial cells)6,使毛細血管產生突發、可逆性通透性增加,血漿蛋白、液體和電解質迅速從血管滲透到組織間隙,在四肢產生末端水腫、肌肉水腫及橫紋肌溶解,在肺部產生肋膜積液及非心因性肺水腫,在腸胃道產生腹瀉與腸胃道水腫,另一方面也因低血容導致低血壓、休克、心搏過速、影響終端器官灌注,造成心、肺、肝等器官損傷,嚴重者甚至會多重器官衰竭甚至死亡1,7。毛細血管滲漏症候群為排除性診斷,易與敗血症、血管性水腫或過敏性休克相混淆7,在此案例醫師診斷排除感染可能,病人於治療期間僅使用口服預防性抗生素 cefadroxil,所有細菌培養包括血液、尿液與痰液等結果皆為陰性,生命徵象在 IL-2給藥前穩定,其他檢驗如肝功能、腎功能、白蛋白、電解質、白血球與血小板數值皆在正常範圍內,不過臨床症狀在給藥後惡化,陸續出現低血壓、心搏過速、周邊水腫、體重增加、腹瀉、肝功能異常、寡尿、血液肌酐酸上升等。臨床症狀通常會在給予每一劑量後加重,但隨著藥物代謝逐漸緩解,此病人在結束五天治療週期後逐漸恢復並出院,治療期間也沒有使用其他目前已知可能會造成毛細血管滲漏症候群藥物。
低血壓是高劑量 IL-2治療中最常見的毒性,約有七成病人發生,與毛細血管通透性增加相關,收縮壓於治療期間會降低20-30 mmHg,但多無臨床症狀,如沒有心血管相關危險因子,可接受的目標收縮壓約為80-90 mmHg,不過在冠狀動脈或腦動脈疾病風險較高病人可以向上調整,而病人有高血壓病史應於治療前立即停用抗高血壓藥物。輸液治療是治療中相當重要部分,若補充不足,會導致低血容量與低血壓影響器官灌流造成損傷,然而輸液補充亦可能會滲漏至血管外加重水腫。因此,為避免液體過載 (fluid overload),補充時應給予足夠復甦的最少量輸液,種類不論是膠體 (colloid) 或晶體 (crystalloid) 輸液皆可給予,補充時需監測血壓與病人水腫狀況,必要時給予升壓劑治療。病人體重於每一治療週期平均增加約5-10%8。如出現嚴重呼吸困難與周邊水腫,於血壓穩定可以給予亨利氏環利尿劑 (loop diuretic)7。
IL-2也可能會產生中樞神經系統毒性,然而其詳細機轉目前仍不清楚,並且可能在沒有給予其他劑量下惡化,因此及早期識別與停止治療相當重要,輕度神經毒性如煩躁不安或失眠,不應導致治療中斷,造成的原因可能是與住院、不活動 (immobility) 或 IL-2使用有關,可考慮使用 benzodiazepine 類藥物治療,但產生嚴重毒性症狀如加重造成人格改變、出現敵意、混亂、定向障礙、幻覺,則可能需使用抗精神病藥物,甚至停止治療。
治療期間也可能會有發燒、寒顫、噁心、嘔吐、腹瀉、皮膚搔癢等不適,治療前可預防性投予 acetaminophen 與 indomethacin 用於退燒、meperidine 用於控制寒顫、prochlorperazine 或5HT3-antagonists 用於止吐、loperamide 用於腹瀉、抗組織胺藥物用於皮膚搔癢及抗生素以避免感染,如出現代謝性酸中毒可給予碳酸氫鈉以維持[HCO3-]大於18 mEq/L,另外也可能會出現輕微肝功能異常、寡尿與血液肌酐酸上升,通常在停藥後可恢復。
由於高劑量 IL-2治療可能會產生嚴重藥物不良反應,病人在接受治療前須作詳細評估與檢查,只有心肺功能完整並且美國東岸癌症臨床研究合作組織 (Eastern Cooperative Oncology Group, ECOG) 體力狀態得分必須為0或1才適合接受治療,通常治療療程 (course) 包含兩段五天治療週期 (cycle),每八小時給予600,000或720,000 IU/kg,一天三次,連續五天,給予十四至十五個劑量,以靜脈輸注超過十五分鐘給藥8,於停藥期後再重複給另一次五天治療週期2,9,如腫瘤消退 (regression) 可考慮接受額外治療週期10,通常相關藥物不良反應在給藥後6小時內發生,並在下一次給藥前逐漸緩解,病人在接受每次給藥前皆需評估臨床狀況是否適合,以確保不良反應逐步改善或消退,如症狀相對輕微可以採取適當處置或跳過該次給藥8。但如症狀嚴重不易恢復,則應停止治療8,11。只有非常少數病人可以接受所有劑量,且在第一週期接受的劑量通常會多於第二週期。本案例因為產生低血壓、肺水腫與呼吸困難等不良反應跳過四次共接受十一個劑量。
在一篇追蹤時間長達12年,分析單一機構以靜脈注射高劑量 IL-2(每8小時720,000 IU/ kg) 治療轉移性黑色素癌及腎細胞癌共1241案例的回溯性研究,作者將最初組155例患者與最終組比較,發現3級和/或4級藥物不良反應發生率顯著降低,治療相關死亡率也由1987年3%下降至1990年以後0%,第一治療週期接受的 IL-2劑量也由1987年平均使用13劑下降至1991年後平均8劑,該研究也比較不同時期的總反應率 (overall response rate) 與持續完全反應率 (ongoing complete response rate),在黑色素癌的p值分別為0.4與1.0,腎細胞癌分別為0.92與0.89,都沒有達到統計學上顯著差異,顯示隨著 IL-2使用經驗累積,儘管病人接受到的劑量降低,但安全性改善並且總反應率與持續完全反應率也沒有受到影響12。
另一篇比較高劑量與低劑量 IL-2用於轉移性腎細胞癌的三臂 (three-arm) 隨機對照研究,該研究先隨機將117名病人分成靜脈注射高劑量 (720,000 IU/kg) 與低劑量 (72,000 IU/kg) 組。之後加入第三組-皮下注射低劑量 (72,000 IU/kg) IL-2,並將後來的283名病人做隨機分配。結果顯示低劑量組產生之相關藥物不良反應 (特別是低血壓) 比率較低,但沒有任何一組有發生 IL-2相關死亡。高劑量組有較高反應率 (21% vs 13%, p = 0.048),不過在總存活期比較並沒有達到統計學上差異。作者利用存活分析比較各組中完全反應者的存活,追蹤132個月後高劑量組仍有九成病人存活,相反地低劑量組僅有五成存活,p = 0.04是有達到統計學上差異,以低劑量 IL-2治療雖然可以減少不良反應發生,不過可能會降低持久抗癌效果13。此外目前研究也發現 IL-2具有雙相作用,除高劑量治療可刺激免疫功能以對抗癌症,於低劑量時會使具有較高 IL-2受體親和力的調節T細胞 (regulatory T cell,Treg) 活化,反而產生免疫抑制功能,可用於避免移植後的排斥反應與血管炎治療14。
肆、結論
毛細血管滲漏症候群是使用高劑量 IL-2治療可能會導致的嚴重藥物不良反應,不過這是與使用劑量相關並且是屬於可以預期的藥物不良反應,在治療前仔細評估病人是否適合接受高劑量 IL-2治療,在接受每次劑量前仔細評估臨床狀況並妥善處理,高劑量 IL-2仍然是癌症免疫療法有效且安全的用藥選擇。
Interleukin-2 (IL-2) Related Capillary Leak Syndrome
Po-Hsien Lu1,
Tzu-Cheng Tsai1,2
Department of Pharmacy, Chang Gung Memorial
Hospital, Linkou1
Department of Long Term Care, Hsin Sheng College
of Medical Care and Management2
Abstract
High-dose interleukin-2(IL-2) is the first immunotherapy approved for the treatment of metastatic renal cell carcinoma and melanoma. It has been shown to consistently induce durable responses in a subset of patients leading to long-term survival. However, high dose interleukin-2 may cause capillary leak syndrome. This leads to an increase in the permeability of capillaries, which causes fluids leak into the interstitial space outside the blood vessels. On the other hand, it also causes hypovolemia, affecting organ perfusion and even death. These adverse drug reactions are dose-dependent, reversible, predictable, and manageable. Therefore, high doses of IL-2 remains an effective and safe treatment option.
參考資料:
1. Jiang T, Zhou C, Ren S: Role of IL-2 in cancer immunotherapy. OncoImmunology 2016;5(6):e1163462.
2. Klapper JA, Downey SG, Smith FO, Yang JC, et al: High-dose interleukin-2 for the treatment of metastatic renal cell carcinoma : a retrospective analysis of response and survival in patients treated in the surgery branch at the National Cancer Institute between 1986 and 2006. Cancer 2008;113(2):293-301.
3. Amin A, White RL: Interleukin-2 in Renal Cell Carcinoma: A Has-Been or a Still-Viable Option? J Kidney Cancer VHL 2014;1(7):74-83.
4. Gills J, Parker WP, Pate S, Niu S, et al: The Role of High Dose Interleukin-2 in the Era of Targeted Therapy. J Urol 2017;198(3):538-45.
5. Rosenberg SA, Yang JC, White DE, Steinberg SM: Durability of complete responses in patients with metastatic cancer treated with high-dose interleukin-2. Ann Surg 1998;228(3):307-19.
6. Krieg C, Letourneau S, Pantaleo G, Boyman O: Improved IL-2 immunotherapy by selective stimulation of IL-2 receptors on lymphocytes and endothelial cells. Proc Natl Acad Sci U S A 2010;107(26):11906-11.
7. Siddall E, Khatri M, Radhakrishnan J: Capillary leak syndrome: etiologies, pathophysiology, and management. Kidney Int 2017;92(1):37-46.
8. Dutcher JP, Schwartzentruber DJ, Kaufman HL, Agarwala SS, et al: High dose interleukin-2 (Aldesleukin) - expert consensus on best management practices-2014. J Immunother Cancer 2014;2:26.
9. Pachella LA, Madsen LT, Dains JE: The Toxicity and Benefit of Various Dosing Strategies for Interleukin-2 in Metastatic Melanoma and Renal Cell Carcinoma. J Adv Pract Oncol 2015;6(3):212-21
10. Payne R, Glenn L, Hoen H, Richards B, et al: Durable responses and reversible toxicity of high-dose interleukin-2 treatment of melanoma and renal cancer in a Community Hospital Biotherapy Program. J Immunother Cancer 2014;2:13.
11. Schwartzentruber DJ: Guidelines for the safe administration of high-dose interleukin-2. J Immunother 2001;24(4):287-93.
12. Kammula US, White DE, Rosenberg SA: Trends in the safety of high dose bolus interleukin-2 administration in patients with metastatic cancer. Cancer 1998;83(4):797-805.
13. Yang JC, Sherry RM, Steinberg SM, Topalian SL, et al: Randomized study of high-dose and low-dose interleukin-2 in patients with metastatic renal cancer. J Clin Oncol 2003;21(16):3127-32.
14. Choudhry H, Helmi N, Abdulaal WH, Zeyadi M, et al: Prospects of IL-2 in Cancer Immunotherapy. BioMed Res Int 2018;1-7.
通訊作者:盧柏先/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 2790