摘要
我國自2016年7月1日開始執行 GDP 查核,2019年1月1日起未通過查核者不得從事相關業務。世界衛生組織 (WHO) 在2010年;歐盟在2013年都訂定優良藥品運銷規範,其中也針對庫存的出庫原則明確規範,即採「效期短者優先出庫 (first expiry/first out;FEFO)」,即俗稱的「先進先出」原則,有任何特例則必須加以記錄並留存相關文獻。
目的:我國確保藥物物流品質的品質保證制度 (優良藥品運銷規範) 早已上路,多數醫療院所總是在相信 GDP 的執行有其一定品質的認知下,理所當然著重在自己院所的管控機制,本院在檢討先進先出作業常規的異常時,發現部分異常可能非醫院內部管理的因素,故著手相關研究。
方法:原有的收貨檢核表上,加註該藥品品項的上一批採購效期,並自2018年12月至2019年3月期間開始統計分析,請收貨人員驗收時,務必記錄當次收貨效期小於前一批效期之品項,並由筆者針對資訊系統的記錄與人工登錄結果進行雙重核對來加以確認,不論物流商的規模及屬性 (跨國性或是台灣地區),就所有效期短於前次收貨之品項數來加以統計分析。
結果:經過4個月的統計 (2018年12月至2019年3月),有入庫之145家物流商總驗收入庫數為2770項,曾出現異常的15家物流商中總驗收入庫數為1624項,標的的異常項次有24項,以項次而言,占該期間總驗收入庫及曾出現異常物流商總入庫項次的百分比分別為0.87%及1.48%。
討論與建議:藥品物流廠商對效期管控應包括 FEFO 原則並納入品質保證的稽核條件,而醫療院所也應重視此類外部因素造成的藥品管理風險,FEFO 的原則必須從製造廠至最終零售調劑的藥局都嚴格遵守,才能確保藥物管理的品質。
關鍵字:優良藥品運銷規範、GDP、效期短者優先出庫、FEFO、good distribution practice (GDP)、first expired/first out (FEFO)
壹、前言
藥物品質的管理,從原料藥、藥廠再到醫療院所,最後送達病人手中;所要監督及管理的細節,從原料藥的來源開始,經過藥廠的製程,成品透過物流運送至醫療院所後,在醫療院所的妥適保存下,最後送到病人的手中,而病人能有正確的服用方式才能達到治療目的。目前絕大數醫療院所的藥劑部門皆對於藥品的管理,從醫院常備藥品品項的選擇、申購、驗收入庫、儲存、出庫...等流程,皆已制定明確的標準作業程序書 (Standard of Practice;SOP) ,不論是醫學中心或其他等級的醫院皆然1,2。由於這些庫存管理 (inventory control;IC) 的觀念已相當成熟;目前有關庫存管理的相關研究方向,其最終目的多聚焦於品質管理或降低成本3-9。(楊晴雲, 2009) 的碩士論文中利用無線射頻識別技術 ((Radio Frequency Identification;RFID) 和條碼 (Barcode) 來建構醫院藥品庫存管理系統3,RFID 或 Barcode 應用的研究在當時如雨後春筍,包括將條碼導入醫材管理、將 RFID 技術應用在 ERP 庫存管理系統、運用 RFID 之食品倉管資料庫管理系統…等。(楊士民等人, 2017) 以品管圈的手法針對進藥作業及備藥流程改善藥庫藥品缺藥問題,降低藥品缺藥率4。 (莊樹義等人, 2016) 為了減少藥庫庫存成本,利用精實醫療,針對耗用量前十大的品項庫存轉移至藥局,探討藥庫局部零庫存成效5。(T. Awaya, 2005) 的研究則顯示利用自動化的資訊系統整合處方、調劑、扣帳、調撥及庫存管理…等藥事作業相較於10年前的電腦作業單機系統將相關的藥事作業負荷減少75%至25%的負荷,可充分減少相關的人事成本6。(R. Findlay 等人, 2015) 利用自動調劑櫃的設定方法加以研究,即分別以「動態庫存管理標準」及「低庫存量警示訊號系統」對照傳統作法,結果發現「低庫存量警示訊號系統」同時可降低庫存量短缺的次數和期間;而「動態庫存管理標準」則僅能降低每天庫存量短缺的次數,最終採用兩種管理方式可降低自動調劑櫃管理的人力及庫存成本7。(Kumar 等人, 2015) 及 (Kivoto 等人, 2018) 分別以藥品耗用量及耗用成本占率將藥品區分為 ABC 三級 (依耗用成本高至低分別為 ABC),再依藥品的重要性區分為非常重要、重要及低重要性三等級來分析發現兩研究中高費用占率的品項的前6.77%及13%左右品項,其分別占總費用的70.03%及79.9%,顯示分類管理對藥品庫存管理的重要性8,9。
有關藥品運送過程的規範,推究其法源,可溯至藥事法53-1條10,國際藥品稽查協約組織 (PIC/S) 亦於2014年6月1日正式公告藥品優良運銷規範 (GDP),我國也參考 PIC/S 組織公告之法規擬訂國內藥品儲存及運銷相關規範,實際上食品藥物管理署 (下稱食藥署) 於2011年度起已規劃逐步推動我國藥品運銷管理制度,自2012至2014年已進行95家廠商之輔導訪查11。我國於2015年7月16日公告「西藥藥品優良製造規範 (第三部:運銷),並於2016年2月18日公告「西藥藥品優良製造規範 (第三部:運銷) 之施行項目及時程」,自2016年7月1日開始執行 GDP 查核,2019年1月1日起未通過查核者不得從事相關業務12。世界衛生組織 (WHO) 2010年也訂定優良藥品運銷規範,其中也針對庫存的出庫原則明確規範,即採「效期短者優先出庫 (first expiry/first out;FEFO)」,即俗稱的「先進先出」原則,並且應優先被採用13。歐盟在2013年11月5日公布的優良藥品運銷規範準則中,同樣規範藥品經銷商必須確保交付給大眾的藥品品質無虞,在準則中提到其庫存的流動必須依照「效期短者優先出庫 (first expiry/first out;FEFO)」的原則,有任何特例則必須加以記錄並留存相關文獻。
貳、目的
儘管多數研究多集中在庫存管理的經濟效益或是新科技應用的效益,而我國確保藥物品質的品質保證制度早已上路,然而物流運送過程是否符合優良藥品運銷規範 (good distribution practice;GDP),多數醫療院所都相信 GDP 的執行有其一定品質,理所當然著重在自己院所的管控機制,在基層的醫療院所內除了要監控上面的條件外,更要管控進到院所藥品的效期。以筆著所在的醫院為例:本院為區域教學醫院,說大不大,說小也不小,身為藥庫管理藥師,依據藥事委員會所通過的品項進行藥品採購,其藥品之來源多數沒有問題,所以藥庫最大的問題會是庫存周轉率的掌控及效期管控;為了精確的掌控藥品的庫存量及效期,本院採取日盤、月盤及年盤,其中日盤及月盤主要是盤點庫存量,年盤則細分為庫存量的盤點及效期兩大項,而效期又細分為效期在一年內及大於一年兩個細項之品項,若屬於效期在盤點日加1年內的日期,則額外再進入電腦系統查詢電腦內的效期是否跟人員所檢視的效期一致。經2017年底所進行的盤點,最後總計85筆中找出有16筆電腦不符,2018年則總計58筆中有8筆電腦不符。管理最基本的精神就是要能追根究底,檢討資訊系統與實際庫存不符合的原因,連續兩年的差異使得我們不得不懷疑人員未落實先進先出的原則,依據電腦先進先出的設定,當進行採購驗收入庫時,正常的情況後入庫之品項的效期一定比前一批長,效期不符表示人員藥品上架時未依順序排定藥品或是取藥時未依先進先出之原則。在此情況下,為了瞭解其真正原因,所以進行此研究。
參、方法
為求徹底解決此類異常,於是要求人員在上架時一定要徹底核對藥品的效期及批號…等資訊,並區隔存放以免未先進先出,嚴格執行此措施後,沒多久就發現廠商本身出貨似乎也存在未落實「效期短者優先出庫 (first expiry/first out;FEFO)」的原則;即筆者所在醫院同一藥品前後入庫的效期本身就存在未先進先出的問題,於是筆者在原有的收貨檢核表上,加註該藥品品項的上一批採購效期 (表一),並自2018年12月開始,請收貨人員驗收時,務必注意當次收貨效期是否小於前一批效期,為了確認統計結果出現人為誤差,此紀錄也會由筆者針對資訊系統的記錄與人工登錄結果進行雙重核對來加以確認,不論物流商的規模及屬性 (跨國性或是台灣地區),所有藥品入庫時皆須逐筆登錄,並記錄至2019年3月。
統計分析:逐日記錄當日總進貨品項、異常品項總數,再就研究期間分析其發生研究目的所描述之異常事件的百分比,並就廠商別分別就所有效期短於前次收貨之筆數加以記錄,當發生於同一出貨廠商時採累計方式留存,藉以統計該廠商之所有物流行為出現就標的事件的百分比。此外,我們亦針對標的期間所有採購入庫廠商加以統計,不論其採購次數多少皆視為一家廠商,以統計在此期間中曾出現本研究之異常事件的廠商占此期間之所有曾採購入庫的廠商百分比。
表一 藥品入庫紀錄表
肆、結果
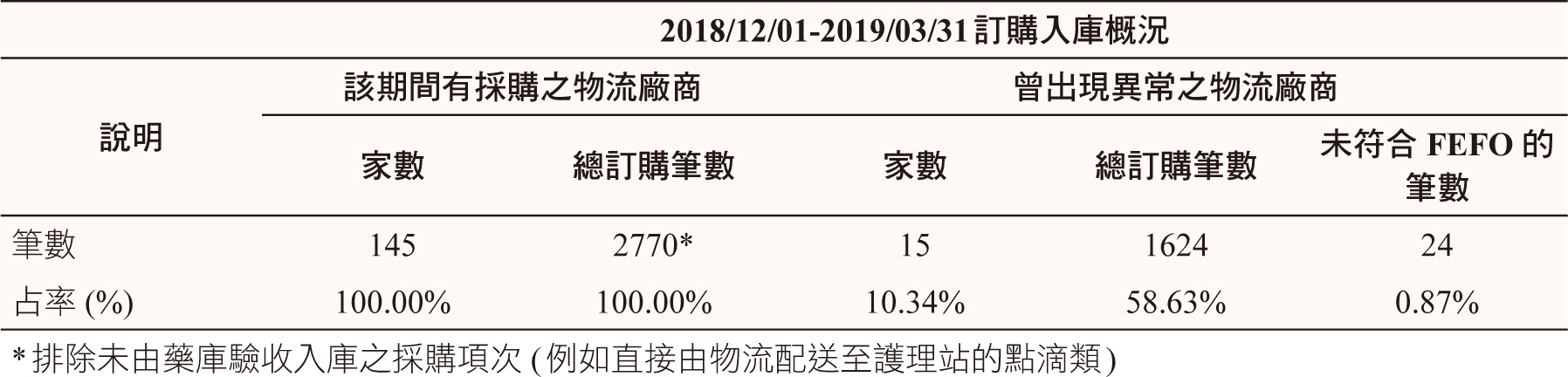
經過4個月的統計 (2018年12月至2019年3月),曾採購至少一個項次並完成入庫驗收的物流廠商家數共145家,其總入庫驗收項次為2770項,其中驗收時至少出現效期小於前一次的項次之異常的物流廠商家數共有15家,約占曾採購入庫之物流商家數的10.34%(表二),而這15家的總入庫驗收項次為1624項 (表二及表三),占該期間總入庫項次的58.63%(表二),而其出現標的異常的項次共有24項次,當中甚至還有1筆其出貨紀錄與入庫藥品批號不符,約占總入庫項次的0.87%(表二),相對占曾出現標的異常之物流商總採購入庫項次的1.48%(24/1624)(表二)。
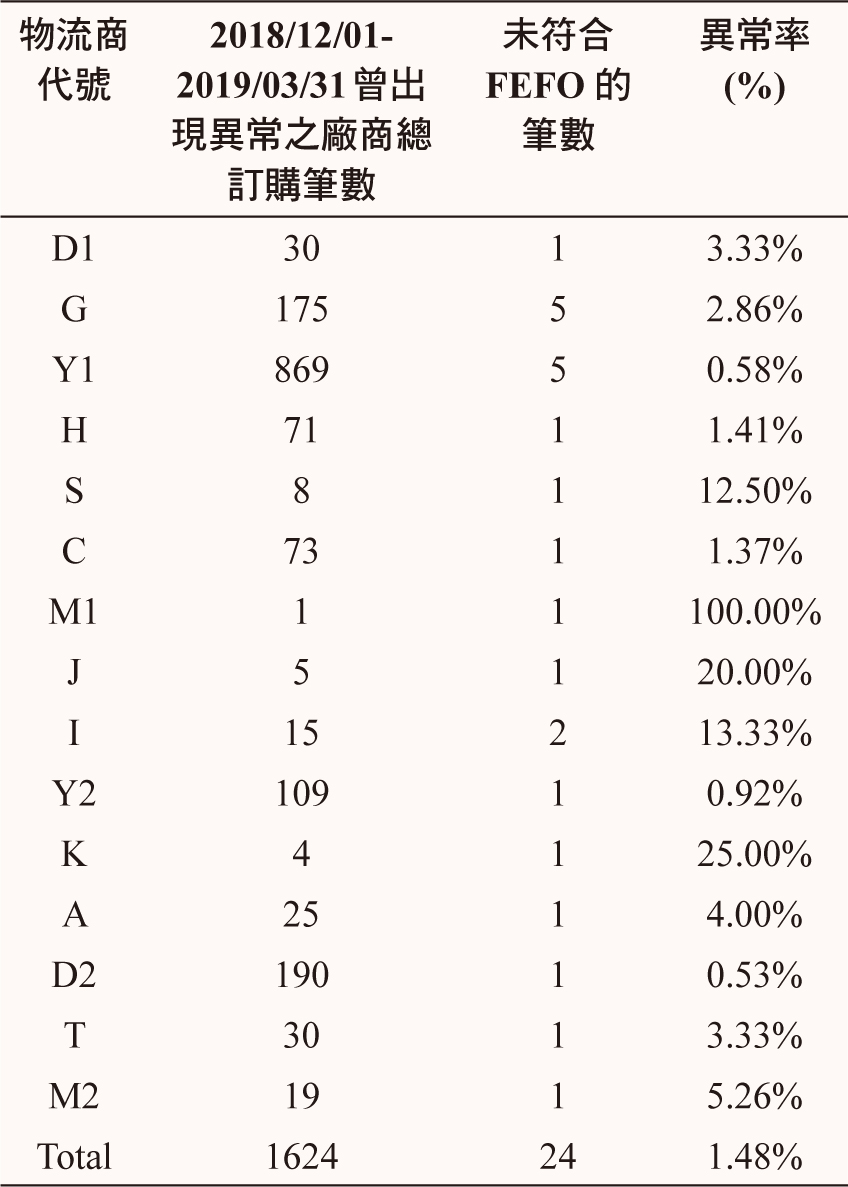
在這些物流商中出現標的異常的次數不只一次的物流商共有3家 (表三),甚至有物流商四個月當中出現達5次之多,包括某家跨國際性的大型物流商,儘管因為其出貨量非常大,故異常率僅為0.58%,但依照 GDP 的精神這也是物流商必須確保的作業品質。
表二 2018/12/01-2019/03/31本院訂購入庫概況分析表
表三 曾出現未符合 FEFO 原則之廠商總訂購筆數及異常筆數一覽表
伍、討論與建議
筆者發現歐盟所謂的例外情況不只一種,姑且不論此次研究目的的事件,例如物流商已知之效期異常 (效期較短),不符本院驗收標準 (訂為效期不足一年) 者,為數亦不少,多數廠商會出具萬一存貨未銷完便過期保證換貨的切結書…等,本院才會勉強驗收,其都攸關藥物品質的管控,在此暫且不討論。
此次研究顯示部份廠商出貨並未依照先進先出的原則,(物流商交貨似乎未採取 FEFO 的原則),有些品項儘管效期超過一年,然而依 GDP 的準則,其確實為一異常事件,筆者無法得知廠商端是否有此資訊,不論其為蓄意或無意,都應納入品質改善的重點,雖然這並非收受端 (醫療院所) 的責任,然而這卻實質影響醫療院所的管理風險;因為院所的管理方式,會慣性地將後入庫的藥品擺在庫存位置之效期較久的區域。從筆者在為期僅4個月的時間就發現24筆較晚收貨驗收之藥品效期較短,這種異常可能使得藥庫端即使依照 FEFO 原則調撥藥品給各分倉 (不論是門診或住院藥局…等) 時,犯了同樣的錯誤,由於政府自2016年即強制所有藥品物流業必須謹守 GDP 原則,此類異常原本就不該出現;但考量本院的業務量並非大量,訂購情況亦不如其他大型院所,卻已有24件之多,依此推論全國的案件數勢必更多。政府政策已經確定2019年1月1日起未通過查核者不得從事相關業務,殊不知吾等所觀察到的異常情況是否攸關物流廠商資格的評核要件。若是,則希望吾等的研究能激起物流廠商對效期管控,包括 FEFO 原則的重視而納入品質保證的稽核條件,果真如此,我國所推動的 GDP 才能與世界衛生組織 (WHO) 於2010年或是歐盟於2013年底就已訂定優良藥品運銷規範達到一致的水準。
此外,更重要的是提醒其他醫療院所重視此類外部因素造成的藥品管理風險,FEFO的原則必須從製造廠至最終零售調劑的藥局都嚴格遵守,才能確保藥物管理的品質。
Risk correlation between Medical Distributors and Hospital Drug Inventory Management
Mei-Chi
Tsai, Tzu-Shun Lin
Pharmacist of Camillians Medical Foundation
Saint Mary’s Hospital, Luodong
Abstract
Taiwan has implemented GDP inspection since July 1, 2016. Those who fail to pass the inspection on January 1, 2019 may not engage in related business. The World Health Organization (WHO) and the European Union has set the quidelines for good drug delivery in 2010 and in 2013 respectively, which also clearly regulates the principles of inventory control, including the principle of first expiry/first out (FEFO), which is commonly known as the "first in, first out (FIFO)" principle. Any special event must be recorded and retained. OBJECTIVE: Taiwan's quality assurance system for ensuring the quality of pharmaceutical products has been on the road for years. Most medical institutions suppose that the implementation of GDP exhibit certain quality, and just focus on the control mechanism of their own institutions. When reviewing the anomalies of the FIFO practices, we found that some of the abnormalities may not be internal factors of the hospital inventory control system, so the relevant research was initiated. METHOD: We modified the original receipt checklist by adding the column of expired day validation of each drug item, and start to collect the data from December, 2007 to March, 108, and ask the inspection personnel to record if the expired day is earlier than previous one of the inspected items as abnormalities, and we would confirms the record of information system with the manual record for double check subsequently, regardless of the properties of distributors (international or Taiwan locally), statistical analysis is carried out based on the number of items the expired day is earlier than previous one of the inspected items versus all items. RESULT: After 4 months of inspection (December 2018 to March 2019), there were 2,770 inspection revenues from total 145 distributors, and 1,624 total revenues from 15 distributors with target abnormalities. There were 24 target items detected, which accounted for 0.87% and 1.48% of the total inspection of all distributors and the total number of targeted distributors respectively during the period. DISSCUSSION and SUGGESTION: the GDP for Drug distributors should include FEFO principles in their quality assurance auditing system, and medical institutions should also pay attention to drug management risks caused by such external factors. FEFO principles must be strictly confirmed from manufacturing to final retail processes, then the pharmacy is able to ensure the quality of drug management.
參考資料:
1. 臺大醫院新竹分院藥庫管理網頁 20190330 https://www.hch.gov.tw/hch/MedicalTeams/CommonFileData.aspx?MNO=C098
2. 高雄市立大同醫院/病人安全藥事作業.pdf http://www.kmtth.org.tw/patient_safe/file/%E8%97%A5%E5%
93%81%E5%AE%89%E5%85%A8%E5%BA%AB%E5%AD%98%E7%AE%A1%E7%90%86%EF%BC%88%
E6%AA%94%E6%A1%88%E4%B8%80%EF%BC%89.pdf
20190330下載
3. 楊晴雲 利用RFID和Barcode建構藥品庫存管理系統–以醫院為例 (2009年碩博士論文) https://hdl.handle.net/11296/thw5a8
4. 楊士民、鄭淑文 以品管專案降低藥品缺藥率 藥學雜誌131冊 2017 年6月出版Vol. 33, No. 2 : http://jtp.taiwan-pharma.org.tw/131/108-112.html
5. 莊樹義…等人 精實醫療探討藥庫局部零庫存成效 藥學雜誌 128冊 2016年9月出版 Vol. 32, No. 3 : http://jtp.taiwan-pharma.org.tw/128/136-141.html
6. Toshio Awaya et al.., Automation in Drug Inventory Management saves Personnel Time and Budget YAKUGAKU ZASSHI 125(5) 427-432.
7. Russell Findlay, et al: Implementation of Advanced Inventory Management Functionality in Automated Dispensing Cabinets Hospital Pharmacy 2015;50(7):603-608.
8. Kivoto PM et al: Clinical and Financial Implications of Medicine Consumption Patterns at a Leading Referral Hospital in Kenya to Guide Future Planning of Care Frontiers in Pharmacology, 10 December 2018 Volume 9 Article 01348 https://doi.org/10.3389/fphar.2018.01348
9. Maj Sushil Kumar et al. ABCeVED analysis of expendable medical stores at a tertiary care hospital Medical Journal Armed Forces India Volume 71, Issue 1, January 2015, Pages 24-27.
10. 藥事法 (民國 107 年 01 月 31 日修訂版) 2019/04/13下載自全國法規資料庫 https://law.moj.gov.tw/LawClass/LawAll.aspx?PCode=L0030001
11. 鍾綺…等人 我國實施藥品優良運銷規範制度之研究 Ann. Rept. Food Drug Res.(食品藥物研究年報) 8期 (2017/11/01) : P323-330.
12. 林中豪…等人 我國推動藥品優良運銷規範(GDP)管理制度與國際接軌之探討 Ann. Rept. Food Drug Res.(食品藥物研究年報) 6 : 406-413 2015.
13. WHO good distribution practices for pharmaceutical products WHO Technical Report Series, No. 957, 2010.
14. European Comission Guidelines of 5 November 2013 on Good Distribution Practice of medicinal products for human use Official Journal of the European Union
15. Dann Salamie Modern inventory analysis techniques Am J Health-Syst Pharm-Am J Health-Syst Pharm. Feb 15, 2000 Vol 57:351-67.
通訊作者:林子舜/通訊地址:宜蘭縣羅東鎮中正南路160號
服務單位:羅東聖母醫院藥劑科藥師/聯絡電話:(O) 03-9544106 ext 5282