乾燥症候群
黎佳琳1、陳惠玉1、蔡慈貞1,2、江俐慧1
1林口長庚紀念醫院藥劑部藥師、2新生醫護管理專科學校
摘要
乾燥症候群 (Sicca syndrome) 是一種慢性且進行性的自體免疫疾病,因淋巴球浸潤導致腺體組織遭受破壞,除了眼睛乾澀與口腔乾燥的症狀外,可能影響腺體外的器官或併發其他自體免疫疾病,最嚴重可能導致淋巴癌。明確的致病機轉尚未完全明瞭,但目前認為可能與基因、病毒感染、免疫反應、性別與荷爾蒙相關。隨著研究進展,開始掌握一些較重要的疾病特徵,2020年EULAR最新的治療建議在初期的診斷是台灣病人較易接受的非侵入性測試,可以更有效地找出潛在病患。
關鍵字: 乾燥症候群、Sicca syndrome、修格蘭氏症候群、Sjögren's Syndrome、EULAR
壹、前言
乾燥症候群 (sicca syndrome,SS),又稱為修格蘭氏症候群(Sjögren's syndrome),因於1933年由瑞典眼科醫師Henrik Sjögren 發現且描述此疾病而得名。乾燥症候群 是一種慢性且進行性的自體免疫疾病,此疾病主要因淋巴球浸潤導致慢性發炎,進而使外分泌腺(如淚腺與唾腺)原本具正常分泌功能的上皮細胞被淋巴細胞取代,導致黏膜乾燥,如眼睛乾澀、口腔乾燥1。
乾燥症候群又可分為原發性或次發性。原發性的臨床表現除了眼睛與口腔的乾燥外,也會影響腺體以外的相關器官,如皮膚、消化系統、關節、腎臟、神經系統等。而次發性乾燥症候群則除了上述症狀外,還有併發其他自體免疫疾病,如類風濕性關節炎(rheumatoid arthritis,RA)、紅斑性狼瘡(systemic lupus erythematosus,SLE)、硬皮症(systemic sclerosis,SSc)1,2。
依據美國-歐洲共識小組(American-European Consensus Group,AECG)的診斷標準,乾燥症候群的盛行率約0.1%-0.6%,而男女發病比例約為1:9。發病年齡層以30-50歲居多,其中停經後婦女發生率又更高3。
貳、病因與致病機轉
乾燥症目前並未發現確切致病機轉,通常認為是多種因素(基因、病毒感染、免疫反應、性別與荷爾蒙)影響發病與疾病進展。
一、 基因
研究指出乾燥症候群可能與編碼主要組織相容性複合體(major histocompatibility complex,MHC)的人類白血球抗原(human leukocyte antigen,HLA)的DR區域有關3。
除了HLA基因以外,與先天免疫相關的如interferon regulatory factor 5(IRF5)、編碼TNFAIP3相互作用的蛋白1(TNIP1),還有與後天免疫相關的基因,包含B lymphocyte kinase(BLK)、IL-12 subunitα(IL12A)、C-X-C Motif Chemokine Receptor 5(CXCR5)等基因皆被認為與乾燥症候群有關連3。
二、 病毒感染
病毒感染被認為是其中一個可能刺激免疫系統導致乾燥症候群的原因。人類嗜T淋巴球病毒(Human T-lymphotropic virus,HTLV)、人類免疫缺乏病毒(Human Immunodeficiency Virus,HIV)及慢性C型肝炎病毒(Hepatitis C virus,HCV) 上述病毒因與乾燥症候群有相似的臨床表現,被認為可能與其相關。而愛潑斯坦-巴爾病毒(Epstein-Barr virus,EBV)則因為在感染時會活化T細胞與B細胞造成組織傷害,被認為與乾燥症候群有關3。
三、性別與荷爾蒙
因男女發生率懸殊,加上停經後婦女為好發族群,近年亦有研究發現雄性荷爾蒙與自體免疫和B細胞數有關,因此性別與荷爾蒙也被認為是乾燥症候群的相關因素3,4。
四、免疫反應
由於乾燥症候群是自體免疫疾病,有研究發現原發性乾燥症候群病人的唾液腺組織(salivary gland tissue)裡,與干擾素(interferon)有關的基因表現是有被提升(upregulate)的,在這些病人中的發炎激素(proinflammatory cytokine)表現量也是較高的。此外B細胞的活化(B cell activation)也是乾燥症候群主要的致病機轉3。
參、診斷
2016年以前,乾燥症候群的診斷由AECG於2002年修訂的診斷準則為主。之後,以美國風濕病協會(American College of Rheumatology,ACR)與歐洲抗風濕性協會(European League Against Rheumatism,EULAR)共同列出新的ACR/EULAR準則為診斷標準。
ACR/EULAR 準則首先納入條件為排除疾病或藥物干擾,病人是否有以下症狀超過三個月,並排除是否有放射治療、後天免疫缺乏症候群等疾病,再以量表評分(表一)。量表分數達4分以上,即診斷為乾燥症候群。2016年的準則與2002年最大的不同為加重唾液腺切片與血漿抗體的比重到3分,這也表示即使致病機轉未完全明瞭,但已經開始得知某些特病的因素與疾病的相關性,藉由更新量表達到更準確的診斷5。
表一
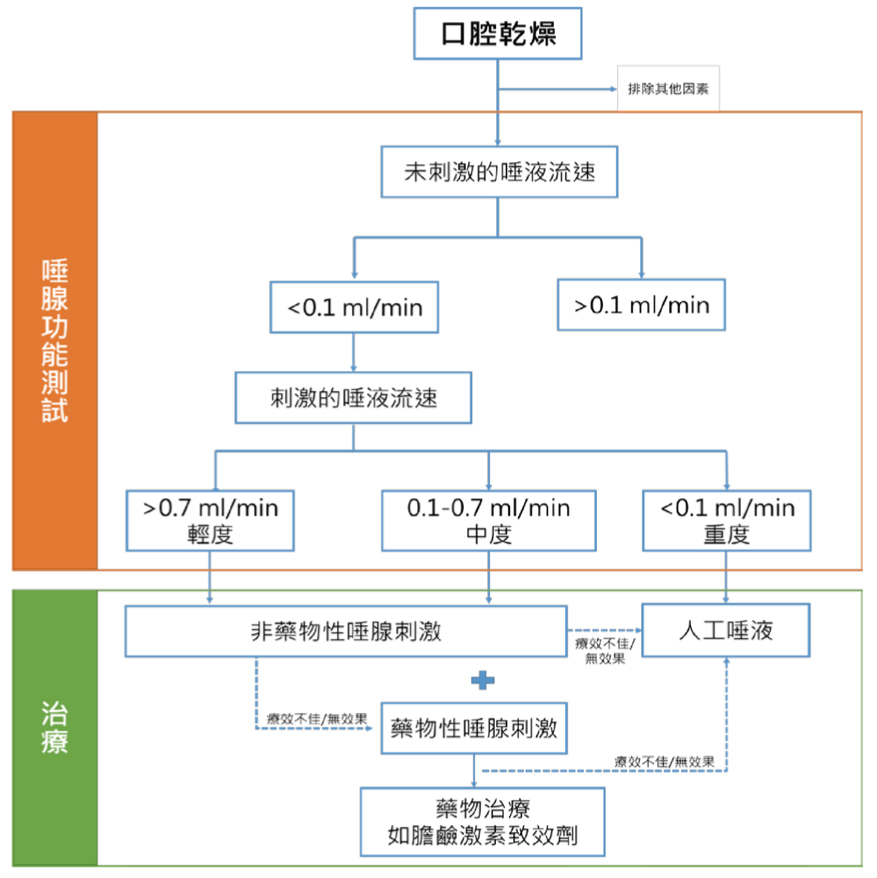
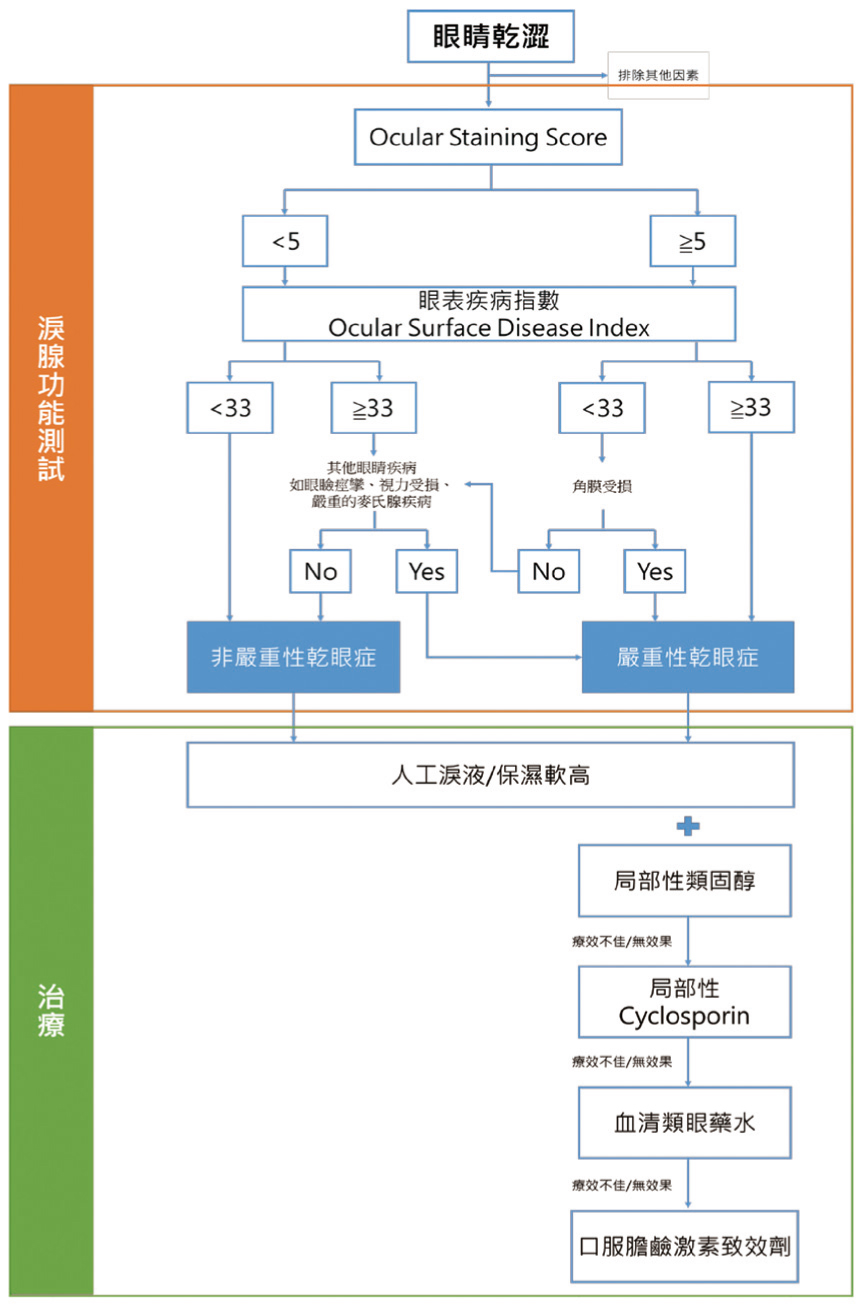
在2020年EULAR發表最新的治療建議中,因應乾燥症候群病人最常出現的眼睛與口腔乾燥問題,做進一步的測試再建議漸進式的治療方法(圖一、圖二)1。同年Chiu YH等人發表的研究指出,由於台灣病人多數較保守,對於2016 ACR/EULAR量表中的唾腺切片的侵入性測試都較為抗拒6。而在眼睛乾燥部分Schirmer's test與乾燥症候群的嚴重性是有相關聯的6。於2020 EULAR治療建議中,以病人接受度較高的進一步非侵入性測試,能幫助診斷出潛在的病人。
圖一
圖二
肆、臨床表現
一、 腺體相關的臨床表現
乾燥症候群主要的臨床特徵為眼睛及口腔的乾燥,病人常有乾性角膜炎(keratoconjunctivitis sicca)、口腔乾燥(xerostomia)、乾眼症(xerophthalmia)等症狀。由於口腔中的唾液分泌減少,唾液無法帶走食物殘渣、保持口腔濕潤,可能引發相關疾病,如口臭、蛀牙、牙周病與念珠菌感染4。其餘如皮膚、陰道等腺體也會被淋巴浸潤,導致乾燥不適。而乾燥症候群病人中大約有30-50%的人會因為唾液腺發炎引起管道阻塞,導致唾液腺腫大(salivary gland enlargement),最嚴重可能導致腮腺淋巴瘤。如同前面提到的,乾燥症候群是一種淋巴球浸潤的疾病,有5-10%的病人疾病可能進展成不同腺體相關的淋巴瘤1,7。
二、腺體外(Extraglandular)的臨床表現
乾燥症候群除了因為淋巴浸潤侵犯腺體外,也如其他自體免疫疾病一樣會產生的自體抗體,如抗核抗體(antinuclear antibody)可能攻擊身體其他的部位,導致如皮膚血管炎(Cutaneous vasculitis)、雷諾氏現象(Raynaud Phenomenon)、間質性腎炎( interstitial nephritis)、關節炎(arthritis)等1,2。
伍、 藥物治療
一、 膽鹼激素致效劑(Cholinergic Agent)
此類藥物透過刺激唾腺和淚腺上的M1和M3受體,抑制因發炎激素(proinflammatory cytokine)造成的細胞凋亡,降低對腺體的傷害以及刺激腺體分泌。Cholinergic agent以症狀緩解為主,目前並無研究發現乾燥症候群是可以被治癒的。常以Pilocarpine 5mg QID 或Cevimeline 30mg TID治療。常見副作用有過度流汗、噁心嘔吐,另外因為藥物對心臟與肺部的作用,有在使用β-blocker與氣喘的病人須注意。依據EULAR建議透過慢慢增加劑量預防的方式,避免最常見的過度流汗副作用1。
二、抗發炎藥物
這類藥物以Cyclosporin為主,透過干擾T細胞的活性,抑制發炎激素(proinflammatory cytokine),來達到作用。一天兩次,以0.05%或0.1%濃度的眼藥水局部給藥8。
三、人工淚液與人工唾液
淚液方面可以用含羧甲基纖維素(carboxymethyl cellulose)或玻尿酸(hyaluronate)成分的人工淚液、凝膠或軟膏劑型1,2,保持眼睛濕潤,降低不適感。唾液有濕潤、抑制細菌的功能,為了避免因口乾導致的相關感染,可使用含羧甲基纖維素(carboxymethyl cellulose)、甘油(glycerin)或黏蛋白(mucin)、山梨糖醇(sorbitol)等成分的人工唾液來保持口腔潤滑與濕潤8。
四、 疾病調節抗風濕藥物(Disease-modifying Antirheumatic Drugs,DMARDs)與類固醇(Steroid)
雖然沒有證據顯示,使用DMARDs可以治療或大幅改善乾燥症候群相關症狀。但是由於乾燥症候群是自體免疫疾病,加上次發性的病人併有其他如RA、SLE等自體免疫疾病,治療上還是會經驗性的使用DMARDS,如Methotrexate,Leflunomide,Sulfasalazine,Hydroxychloroquine1,9。Leflunomide治療由100mg起始劑量(loading dose)開始,一天一次,服用3天後,以10mg-20mg一天一次,Sulfasalazine 500-1000mg QD-BID,Hydroxychloroquine治療由 400mg 起始劑量(loading dose)開始,維持劑量建議為200 or 400 mg。常用的類固醇為Prednisolone,建議使用時間越短越好1。
五、生物製劑(Biologic Agent)
許多研究發現乾燥症候群與B細胞過度活化有關,加上乾燥症候群可能惡化成淋巴癌,有研究嘗試以治療淋巴癌或是RA、SLE的生物製劑治療乾燥症候群。主要使用以B細胞為標靶的抗CD20(anti CD20)跟抗B細胞活化因子(anti B cell activating factor,anti BAFF)的生物製劑治療。但由於目前有關生物製劑的治療皆為仿單外使用(off label used),在治療上的花費較高,須衡量病患經濟能力與疾病對生活造成的影響程度衡量是否使用。
(一) Rituximab
Anti CD20中最常研究的為Rituximab。Rituximab是第一個被核准應用於B細胞淋巴癌的anti CD20單株抗體。透過B細胞在分化過程中會表現CD20,而最終分化的漿細胞不會表現的特點,可以以CD20作為標靶,攻擊癌細胞。在許多的開放式研究(open-label study)以及隨機對照試驗(randomized controlled trial, RCT)中,以每周375 mg/m2,連續使用一個月或是隔週使用1g,持續一個月的劑量,病患自覺眼睛乾澀、口腔乾燥與疲倦是有效改善的10,11。
(二) Belimumab
Belimumab是anti BAFF的單株抗體,核准於治療SLE。有open-label study以10mg/kg的劑量治療乾燥症候群,其中30%的病人認為乾燥症與疲倦有改善10。
陸、 結語
乾燥症候群是一種慢性,進行性的自體免疫疾病,主要的症狀為眼睛口腔的乾燥,但不一定每位病人初發病時都有兩者情況,且容易與其他疾病的症狀混淆,造成診斷上的困難。2020年EULAR在初期的眼睛口腔乾燥診斷上較為細膩,也因為非侵入性測試的特性使病人不易抗拒。根據近幾年對疾病較多的了解,提高了某些項目的比重,希望能更明確地找出病人及早治療。隨著病因逐漸明瞭加上生物製劑的進步,病人未來可以有更多治療上的選擇。而未來的挑戰將是能否找出特定的受體讓病人可以更精準的使用藥物治療。
Sicca Syndrome
Chia-Lin Li1, Hui-Yu Chen1, Tzu-ChengTsai1,2,
Li-Huei Chiang1
1Department of Pharmacy, Chang Gung Memorial
Hospital, Linkou
2Hsin Sheng Junior College of Medical Care and
Management
Abstract
Sicca syndrome is a chronic, and progressive autoimmune disease. Glandular tissue such as salivary gland and lachrymal gland is destroyed due to lymphocyte infiltration. The worse thing that it may also be associated with other autoimmune disorder. There is an increased risk of sicca syndrome develop to lymphoma. Although the pathogenesis remains unclear, sicca syndrome is believed to be related to gene, viral infection, immune reaction and hormone. New recommendation and diagnosis published in 2020 by European League Against Rheumatism (EULAR) applied non-invasive measurement which is widely acceptable by patients in Taiwan. Due to the increasing knowledge of this disorder, dspite none of new treatment develop, novel biological agents used for lymphoma can be possible choices.
參考資料:
1. Ramos-Casals M, Brito-Zerón P, Bombardieri S, et al. EULAR recommendations for the management of Sjögren’s syndrome with topical and systemic therapies. Annals of the rheumatic diseases 2020;79:3-18.
2. Brito-Zerón P, Baldini C, Bootsma H, et al. Sjögren syndrome. Nature Reviews Disease Primers 2016;2:16047.
3. Nocturne G, Mariette X. Advances in understanding the pathogenesis of primary Sjögren's syndrome. Nature reviews Rheumatology 2013;9:544-56.
4. Wilhelmson AS, Lantero Rodriguez M, Stubelius A, et al. Testosterone is an endogenous regulator of BAFF and splenic B cell number. Nature communications 2018;9:2067.
5. Le Goff M, Cornec D, Jousse-Joulin S, et al. Comparison of 2002 AECG and 2016 ACR/EULAR classification criteria and added value of salivary gland ultrasonography in a patient cohort with suspected primary Sjögren's syndrome. Arthritis research & therapy 2017;19:269.
6. Chiu YH, Szu-Hsien Lee T, Chao E, et al. Application of classification criteria of Sjogren syndrome in patients with sicca symptoms: Real-world experience at a medical center. Journal of the Formosan Medical Association = Taiwan yi zhi 2020;119:480-7.
7. Nocturne G, Mariette X. Sjögren Syndrome-associated lymphomas: an update on pathogenesis and management. British Journal of Haematology 2015;168:317-27.
8. Ames P, Galor A. Cyclosporine ophthalmic emulsions for the treatment of dry eye: a review of the clinical evidence. Clinical investigation 2015;5:267-85.
9. Carsons SE, Vivino FB, Parke A, et al. Treatment Guidelines for Rheumatologic Manifestations of Sjögren's Syndrome: Use of Biologic Agents, Management of Fatigue, and Inflammatory Musculoskeletal Pain. Arthritis care & research 2017;69:517-27.
10. Del Papa N, Vitali C. Management of primary Sjögren's syndrome: recent developments and new classification criteria. Therapeutic advances in musculoskeletal disease 2018;10:39-54.
11. Isaksen K, Jonsson R, Omdal R. Anti-CD20 treatment in Primary Sjögren's Syndrome. Scandinavian Journal of Immunology 2008;68:554-64.
通訊作者:江俐慧/通訊地址:桃園市龜山區復興街五號
服務單位:臺北市林口長庚醫院臨床藥學科/聯絡電話:(O) 03-3281200 ext 3730