轉移性大腸直腸癌精準治療
黃喬凱1、楊雅筑2、林佩姿3、李讚紘4
1嘉義長庚醫院藥劑科、2高雄長庚醫院藥劑科、3大里仁愛醫院藥劑科、
|4建合診所大腸直腸外科
摘要
精準醫療是以個人化為出發點,根據每個人的基因選擇最適當的疾病治療方法,達到較為有效、安全、跟最小花費的一種醫療概念。近年來對於轉移性大腸直腸癌的精準治療有更多發現,臨床上可依照基因型給予不同的治療藥物組合,當RAS原生態、BRAF突變,可使用EGFR抑制劑合併BRAF抑制劑及MEK 抑制劑;癌細胞HER2過度表現,可使用含HER2抑制劑trastuzumab的治療組合;癌細胞呈微衛星不穩定/DNA錯誤配對修復機制高度缺陷狀態,可使用免疫檢查點抑制劑;神經營養酪胺酸受體激酶基因融合型態,可使用TRK抑制劑。本文將簡介以上四種轉移性大腸直腸癌精準治療的治療成效。
關鍵字: 精準醫療、轉移性大腸直腸癌、precision medicine、metastatic colorectal cancer
壹、 前言
化療組合FOLFOX(folinic acid/fluorouracil/oxaliplatin)和FOLFIRI(folinic acid/fluorouracil/irinotecan)為現行轉移性大腸直腸癌(metastatic colorectal cancer,mCRC)的一線標準治療。從2004年起1,標靶治療為臨床照護提供了更多的治療選擇並帶來較佳的療效,包含抗血管內皮生長因子(vascular endothelial growth factor,VEGF)、表皮生長因子受體(epidermal growth factor receptor,EGFR)抑制劑等。近年來,隨著檢驗技術的進步、人工智慧的介入,精準醫療(precision medicine)的概念開始應用在臨床上,精準醫療是以個人化為出發點,根據每個人的基因、生活環境跟生活方式選擇最適當的疾病治療方法,達到較為有效、安全、與最小花費的一種醫療概念,並能協助早期疾病診斷與預防。最近有許多臨床試驗證實,mCRC若檢驗出特定幾種基因型或突變狀態,例如BRAF是否突變、HER2是否過度表現、DNA錯配修復功能缺陷(deficient mismatch repair,dMMR)/癌細胞微衛星高度不穩定 (high microsatellite instability,MSI-H)及神經營養性原肌球蛋白受體激酶基因融合(neurotrophic tyrosine receptor kinase, NTRK fusion),對於相對應的治療會有較高的反應率。本文將探討mCRC的精準治療,並聚焦在上述四種特定基因型的藥物治療策略及其效果。
貳、 藥物治療選擇
一、 BRAF突變
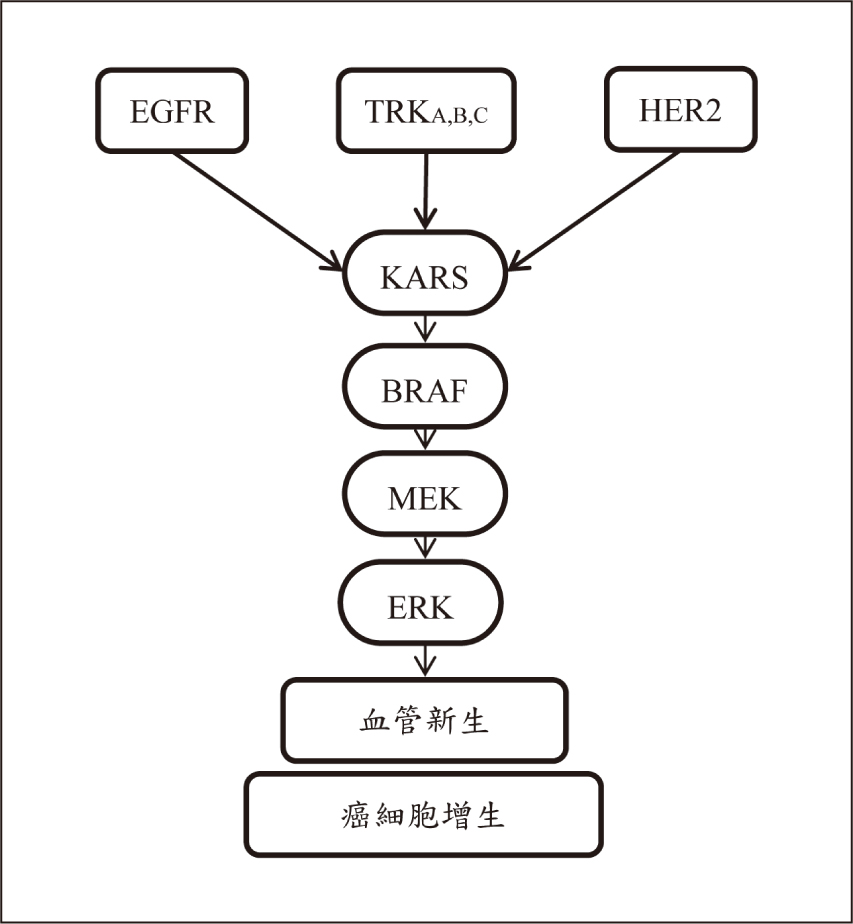
BRAF是影響KRAS-BRAF-MEK-ERK細胞訊息傳遞的基因之一(可參考圖一),常見的突變型為BRAF V600E,BRAF突變有較差的預後且容易轉移。RAS原生態的mCRC常使用EGFR抑制劑(cetuximab或panitumumab)合併化療作為治療選擇,但過去的證據顯示,當RAS為原生態,但發生BRAF 突變,單獨使用EGFR抑制劑會導致治療失敗,因此建議發生BRAF V600E突變的mCRC除使用EGFR抑制劑外,需再合併BRAF抑制劑(encorafenib、dabrafenib)及MEK 抑制劑(binimetinib、trametinib)治療。
圖一 可能造成大腸直腸癌細胞突變的訊息傳遞路徑1
BEACON CRC2為一開放型第三期臨床試驗,共收錄665位先前都曾治療過但仍惡化的BRAF V600E突變之mCRC病人,以1:1:1的方式隨機將病人分成三組:三合一治療組為224人使用cetuximab(起始劑量400 mg/m2,維持劑量每週250 mg/m2) 合併encorafenib (每日一次300 mg)及binimetinib(每日兩次45 mg)、二合一治療組220人,給予cetuximab 合併encorafenib及控制組221人以cetuximab加上一般化學治療(irinotecan 或 FOLFIRI)來治療。三組中位存活期(median overall survival,median OS)分別為9.0月、8.4月和5.4月;整體反應率(overall response rate)分別為26%、20%和2%;六個月存活率分別為 71%、65%和47%,3級以上的不良反應發生率各為58%、50%和61%,其他較常見的不良反應為腹瀉、噁心、嘔吐、痤瘡樣皮疹以及貧血和血紅素低下2。在生活品質上,使用癌症患者生命質量測定量表(EORTC QLQ C30) 和大腸直腸癌病人癌症治療功能性評估量表(Functional Assessment of Cancer Therapy Colon Cancer)評估,發現與控制組相比,三合一治療組能減少45%(HR 0.55,95% CI: 0.43,0.70 )和 44%(HR 0.56,95% CI: 0.44,0.71)的生活品質惡化;而二合一治療組則能減少46%(HR 0.54,95% CI: 0.43,0.69)和43%(HR 0.57,95% CI: 0.45,0.72)的生活品質惡化,使用其他的評估量表,如:歐洲五維健康量表(EuroQol 5D 5L)、病人總體印象變化(Patient Global Impression of Change)量表都有類似的結果,三合一治療組和二合一治療組相較於控制組有較佳的生活品質,但是兩組之間並無顯著差異3。目前美國食品藥物管理局已核准encorafenib合併cetuximab用於BRAF突變型的mCRC病患,且2020年美國國家癌症資訊網(National Comprehensive Cancer Network, NCCN)指引也建議將encorafenib合併cetuximab列為這一族群病人第一線治療選擇4,台灣目前僅有dabrafenib及trametinib,須事前申請,且尚未核准在mCRC上。
另一開放性第一期臨床試驗中,收錄142位BRAF V600E突變的 mCRC病人,將病人分成三組,第一組為panitumumab合併dabrafenib及trametinib,共91位;第二組給予panitumumab合併dabrafenib,共20位;第三組使用panitumumab合併trametinib,共31位,panitumumab劑量為每兩週施打4.8或6 mg/kg、dabrafenib為固定劑量一天兩次150 mg、trametinib為一天一次1.5或2 mg。研究顯示overall response rate分別為21%、10%及0%,以合併三種藥物的反應率最佳;中位疾病無惡化存活期(median progression free survival,median PFS)分別為4.2個月、3.5個月及2.6個月,亦是三種藥物的組合為較長5。
二、 HER2過度表現
HER2是一種生長因子,和大腸直腸癌疾病進展有關,大約有2-6%的mCRC會有HER2過度表現6,許多研究將trastuzumab搭配其他也能抑制HER2過度表現的藥物如:pertuzumab或lapatinib合併使用在HER2過度表現的mCRC上,發現有不錯的治療效果及耐受性。
MyPathway6為一開放、多籃型(multiple basket study)非隨機的第2a期臨床試驗,收錄57位HER2過度表現之難治型mCRC病人,觀察使用trastuzumab(起始劑量為8 mg/kg,維持劑量為每三週6mg/kg)合併pertuzumab(起始劑量為840 mg,維持劑量為每三週420 mg)之療效。研究結果顯示客觀反應率(objective response rate)為32%,其中包含了1位(2%)完全反應及17位(30%)部分反應。研究期間常見不良反應有腹瀉(33%)、疲倦(32%)及噁心(30%);有37%病人發生第3至4級不良反應,以低血鉀及腹部疼痛較常見;有18%發生嚴重不良反應,其中4%為藥物相關不良反應如寒顫和輸注反應;沒有治療導致死亡的案例6。
HERACLES7為一開放型、第2期臨床試驗,收錄27位KRAS原生型,且HER2呈陽性反應的難治型mCRC病人,觀察trastuzumab(起始劑量為4 mg/kg ,維持劑量為每週2 mg/kg)合併lapatinib(每天1000 mg)之療效,其中74%曾經用過4線以上的治療,100%曾使用panitumumab 或cetuximab。治療94週後,objective response rate為30%(8位),其中包含了1位(4%)完全反應及7位(26%)部分反應;median PFS為21週、median OS可達46週。於治療期間無4級以上不良反應,亦無嚴重副作用;僅22%病人出現3級不良反應,包含疲倦、皮膚紅疹及膽紅素升高7。以上研究皆顯示以trastuzumab為底,併用另一HER2藥品治療,或許對HER2過度表現且先前治療無效的大腸癌病人會是一個新契機。但台灣目前不論是trastuzumab、pertuzumab或是lapatinib都尚未核准使用在mCRC的病人上,若臨床上有使用需求,需自費使用。
三、 癌細胞dMMR或MSI-H狀態
約有15%的大腸直腸癌為高度微衛星不穩定(MSI-H)狀態8,微衛星是基因體中的重複排列序列,在DNA複製的過程中容易發生錯誤,在錯誤配對修復系統中若出現缺陷(mismatch repair deficiency,dMMR),錯誤不斷累積就會形成高度微衛星不穩定。
當癌細胞為MSI-H/dMMR狀態的mCRC對於免疫檢查點抑制劑有獨特的敏感性,可單一使用第一類程序性細胞死亡蛋白質(programmed death receptor 1 ,PD-1)抑制劑如pembrolizumab、nivolumab或是PD-1抑制劑合併第四類細胞毒殺T細胞抗原(cytotoxic T-lymphocyte antigen 4,CTLA-4)抑制劑如nivolumab合併ipilimumab4。
CheckMate 1429為一開放型、非隨機第二期臨床試驗,收錄74位經由病理組織顯示為dMMR/MSI-H狀態,且先前至少接受一種治療包含fluoropyrimidine 、oxaliplatin 或irinotecan後疾病持續惡化或無法耐受先前的治療之mCRC病人,每兩週給予3mg/kg的nivolumab,直到疾病惡化、死亡、無法忍受副作用或離開試驗,追蹤期中位數12個月時,有23位病人(31.1%)達到研究者評估的客觀反應(investigator-assessed objective response);51位(68.9%)病人疾病獲得控制達12週以上;所有受試者在分析期間皆存活且有8位對治療持續有反應達12個月以上。研究中最常出現的藥物相關不良反應為疲勞(21.6%)、腹瀉(20.3%)、搔癢(13.5%)和紅疹 (10.8%),最常見的第三級和第四級不良反應為lipase(8.1%)和amylase(2.7%)上升,因ALT(alanine aminotransferase)上升、結腸炎、十二指腸潰瘍、急性腎功能損傷、胃炎而停藥的各有1位,而研究期間有23位(31.1%)病人死亡,但並非藥物導致,研究建議在這類病人上,nivolumab可為治療選項之一9。
KEYNOTE-17710為一開放型、隨機第三期臨床試驗,收錄307位癌細胞狀態皆為dMMR或MSI-H的mCRC病人,將病人隨機分成兩組,第一組共153位受試者,每三週施打200mg的pembrolizumab長達2年;第二組則給予傳統化療共154位。研究顯示第12個月的無惡化存活率分別為55.3%及37.3%;第24個月的無惡化存活率為48.3%和18.6%;客觀存活率兩組依序為43.8%及33.1%;而3-5級治療相關副作用,兩組發生率分別為22%及 66%。整體而言,pembrolizumab與傳統化療相比,已被證實可減少40%的疾病惡化風險且相關副作用較低。
CheckMate-142 11,收錄119位dMMR/MSI-H mCRC病人,其中76%之前曾接受二種以上全身性治療,包含fluoropyrimidine、oxaliplatin、irinotecan、VEGF抑制劑、EGFR抑制劑、regorafenib、trifluridine/tipiracil等。每三週給予病人3mg/kg nivolumab合併1mg/kg ipilimumab,施打四次之後,改為每兩週給予nivolumab 3mg/kg,追蹤期中位數13.4個月時,有65位病人(55 %)達到investigator-assessed objective response;且有95位病人(80%)疾病控制達12週以上;試驗的第9個月無惡化存活率為76%、第12個月為71 %、整體存活率可達87%及85 %。研究中最常見藥物相關不良反應為腹瀉(22%)、疲勞(18%)和搔癢(17%),出現第三級和第四級藥物不良反應比例為32%,多數為AST或ALT數值上升(11%)、lipase上升 (4%)、貧血(3%)及腸炎(3%),有13%的病人因藥物相關不良反應而停藥11。研究中也提到,將nivolumab合併ipilimumab的組合和單一使用nivolumab或pembrolizumab間接比較後發現,nivolumab合併ipilimumab在12個月的客觀反應、PFS和OS都相對較高,在此臨床好處大於風險的情形下,nivolumab合併ipilimumab可望成為MSI-H/dMMR狀態的mCRC病人新的治療選擇。但台灣目前nivolumab、pembrolizumab或是ipilimumab都尚未核准使用在mCRC的病人上,若臨床上有使用需求,則需自費使用。
四、 神經營養性原肌球蛋白受體激酶基因融合(NTRK Fusion)
神經營養酪氨酸受體激酶基因有三種亞型,分別是NTRK1、NTRK2、NTRK3,正常狀況下對於神經系統的發育和功能展現非常重要,但NTRK基因融合會導致原肌球蛋白受體激酶(tropomyosin receptor kinase,TRK)信號持續傳遞,活化TRK嵌合蛋白並使其大量表現,進而造成細胞發育異常並且癌化,目前研究顯示NTRK基因融合陽性者僅占大腸直腸癌<1%1,不過若檢測出此基因融合的病患可考慮使用具高度選擇性的TRK抑制劑larotrectinib或entrectinib,TRK抑制劑可用於具TRK融合的所有癌別包含CRC,皆具有高度反應率且無嚴重副作用出現。
在一研究中12,收錄55位NTRK基因融合陽性病人,年齡介於4個月到76歲間,包含17種癌別,其中有4位為大腸癌。給予青少年或成人larotrectinib劑量為每日口服兩次100mg,對於體表面積小於1m2的兒童則劑量調整為每日兩次100 mg/ m2,服用藥品直到疾病惡化、死亡或產生無法接受的副作用。研究結果顯示overall response rate為75%,追蹤一年後仍有71%,其中55%的受試者仍無疾病惡化。研究中大部分副作用為1至2級不良反應,最常見為ALT及AST上升(42%)、疲倦(36%)及嘔吐(33%);僅少數出現貧血、嗜中白血球減少等3至4級不良反應;沒有病人因藥物相關不良反應而停藥。此研究顯示larotrectinib針對NTRK基因融合陽性的固體腫瘤具有顯著的效果,且不受限年紀及癌別限制。
於一使用entrectinib於NTRK基因融合陽性固態腫瘤的資料庫研究,收錄了54位18歲以上的病人,其包含了10種癌別(其中4位為大腸癌),每日一次給予口服entrectinib至少600mg,追蹤期中位數為12.9個月時, objective response rate 為57%,其中包含了4位(7%)完全反應及27位(50%)部分反應,受試者對於此藥品持續反應時間中位數為10個月,median PFS為11.2個月,median OS為 21個月。在試驗期間較常出現的3至4級的不良反應為體重增加(10%)及貧血(12%);出現較嚴重治療相關的副作用比例為10%,多為神經系統相關副作用(4%)13。雖然這兩藥品對於NTRK基因融合效果顯著,但台灣目前僅有larotrectinib取得藥證。
參、 結論
大腸直腸癌治療會依照癌症的分期及腫瘤位置選擇手術、放射治療及藥物治療,其中藥物的選擇又包含化學治療、標靶治療。隨著基因檢測的技術進步,發現了大腸直腸癌具有不同的基因突變或形態,並依照各個型態選擇精準治療以提升治療效果。期望未來能將大腸直腸癌的個別基因型研究更加透徹,將利於後續針對各種不同基因型選擇更精準的藥物治療。
Precision Medicine of Metastatic Colorectal Cancer
Ciao-Kai Huang1, Ya-Zhu Yang2, Pei-Tzu Lin3, Tsan-Hung Lee4
1Department of pharmacy, Chang Gung Memorial
Hospital, Chia-yi
2Department of pharmacy, Chang Gung Memorial
Hospital, Kaohsiung
3Department of pharmacy, Jen Ai Chang Gung
Health
4Jian Heo Clinic
Abstract
Based on gene, precision medicine is a more effective and safer medical approach to tailor disease treatment for metastatic colorectal cancer (mCRC). In recent years, there have been more discoveries about the precision medicine of mCRC. Thus, in clinical practice, physicians could choose treatments according to the genotype of patients. For example, for patients suffering from mCRC with BRAF mutation, an anti-EGFR agent combining with a BRAF inhibitor and a MEK inhibitor could be an option; for patients with HER2-amplified gene type, trastuzumab is directed against the HER-2 receptor; for patients with mismatch repair deficiency/ high microsatellite instability, immune checkpoint inhibitor is a choice; and for those with neurotrophic tyrosine receptor kinase fusion, tropomyosin receptor kinase inhibitor may have a role. The aim of this review is to discuss the effectiveness of the above four kinds of precision medicine for metastatic colorectal cancer.
參考資料:
1. Guler I, Askan G, Klostergaard J, et al:Precision medicine for metastatic colorectal cancer: an evolving era. Expert Rev Gastroenterol Hepatol, 2019. 13(10):919-931.
2. Kopetz S, Grothey A, Yaeger R, et al:Encorafenib, Binimetinib, and Cetuximab in BRAF V600E-Mutated Colorectal Cancer. N Engl J Med, 2019. 381(17):1632-1643.
3. Kopetz S, Grothey A, Cutsem EV, et al:Encorafenib plus cetuximab with or without binimetinib for BRAF V600E-mutant metastatic colorectal cancer: Quality-of-life results from a randomized, three-arm, phase III study versus the choice of either irinotecan or FOLFIRI plus cetuximab (BEACON CRC). J Clin Oncol 2020. 38(15_suppl):4039-4039.
4. Network NCC. Colon cancer (version 4.2020). June 15,2020]; Available from: https://www.nccn.org/professionals/physician_gls/pdf/colon.pdf.
5. Corcoran RB, André T, Atreya CE, et al:Combined BRAF, EGFR, and MEK Inhibition in Patients with BRAF(V600E)-Mutant Colorectal Cancer. Cancer Discov, 2018. 8(4):428-443.
6. Meric-Bernstam F, Hurwitz H, Raghav KPS, et al:Pertuzumab plus trastuzumab for HER2-amplified metastatic colorectal cancer (MyPathway): an updated report from a multicentre, open-label, phase 2a, multiple basket study. Lancet Oncol, 2019. 20(4):518-530.
7. Sartore-Bianchi A, Trusolino L, Martino C, et al:Dual-targeted therapy with trastuzumab and lapatinib in treatment-refractory, KRAS codon 12/13 wild-type, HER2-positive metastatic colorectal cancer (HERACLES): a proof-of-concept, multicentre, open-label, phase 2 trial. Lancet Oncol, 2016. 17(6):738-746.
8. Gatalica Z, Vranic S, Xiu J, et al:High microsatellite instability (MSI-H) colorectal carcinoma: a brief review of predictive biomarkers in the era of personalized medicine. Fam Cancer, 2016. 15(3):405-12.
9. Overman MJ, McDermott R, Leach JL, et al:Nivolumab in patients with metastatic DNA mismatch repair-deficient or microsatellite instability-high colorectal cancer (CheckMate 142): an open-label, multicentre, phase 2 study. Lancet Oncol, 2017. 18(9):1182-1191.
10. Andre T, Shiu K-K, Kim TW, et al:Pembrolizumab versus chemotherapy for microsatellite instability-high/mismatch repair deficient metastatic colorectal cancer: The phase 3 KEYNOTE-177 Study. 2020. 38(18_suppl):LBA4-LBA4.
11. Overman MJ, Lonardi S, Wong KYM, et al:Durable Clinical Benefit With Nivolumab Plus Ipilimumab in DNA Mismatch Repair-Deficient/Microsatellite Instability-High Metastatic Colorectal Cancer. J Clin Oncol, 2018. 36(8):773-779.
12. Drilon A, Laetsch TW, Kummar S, et al:Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children. N Engl J Med, 2018. 378(8):731-739.
13. Doebele RC, Drilon A, Paz-Ares L, et al:Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol, 2020. 21(2):271-282.
通訊作者:黃喬凱/通訊地址:嘉義縣朴子巿長庚二路20號6樓2
服務單位:嘉義長庚紀念醫院藥劑科/聯絡電話:(O) 05-3621000 ext. 2785