標靶藥物導致手術傷口併發症探討
闕昌琪、王明賢
亞東紀念醫院藥學部
摘要
在傷口癒合的機制中,血管內皮生長因子扮演最重要的促血管生成因子之一,而部份標靶藥物作用機轉與抑制血管內皮生長因子有關,進而會影響傷口的癒合,故傷口併發症是使用標靶藥物治療可能出現的副作用。目前未有探討標靶藥物導致傷口之綜論,各別藥物需要注意之事項不同,因此藉由本文探討此類標靶藥物,於手術前後之處置方式,包括停藥時間、手術後恢復藥物時機等,提出相關建議以供臨床參考選擇,增加用藥安全。
關鍵字: 標靶藥物、傷口癒合、血管內皮生長因子、血管新生
壹、前言
雖然標靶癌症治療的副作用可能較傳統化學治療輕微,但它們也是存在副作用。標靶治療的具體副作用將取決於所使用的藥品,常見副作用包括:皮膚問題,如皮疹、皮膚乾燥、瘙癢、發紅和皮膚角質化,頭髮生長的變化,疼痛敏感化,手腳的發紅腫脹(稱為手足症候群),頭髮或皮膚顏色變化,高血壓,出血或凝血影響,和傷口癒合等,本文主要探討傷口癒合之問題。
貳、傷口癒合機制
傷口癒合機制分急性和慢性。急性傷口癒合涉及細胞和分子的反應,包括(a)免疫系統: 在最初免疫細胞遷移到傷口部位,除了清除入侵病原體外,另外還協調了癒合過程。(b)再上皮化:切割表皮細胞邊緣調節傷口相關基因,啟動集體細胞遷移。(c)纖維母細胞:局部和血源性纖維母細胞增生和遷移形成傷口肉芽組織,提供結構和信號及產生新的癒合基質,部份纖維母細胞可分化成肌纖維母細胞以幫助傷口收縮。(d)血管新生:經由血管新生產生新血管,提供傷口床氧氣和營養。(e)神經分配:傷口癒合和神經分配呈正相關,但過度神經分配在傷口閉合後會導致神經性疼痛。
慢性傷口癒合經常會因感染而持續發炎反應,導致再上皮化失常,傷口角質細胞過度增生,肉芽組織缺陷並且不會促進癒合。部份原因是基質金屬蛋白酶(matrix metalloproteases)升高和纖維母細胞浸潤不良。新的血管生成不良,纖維蛋白圍繞在現有血管外圍,限制氧氣通過傷口,使傷口缺氧。1
參、 血管內皮生長因子(Vascular Endothelial Growth Factor, VEGF)跟傷口癒合的關聯性
新血管形成對於成功修復組織扮演很重要的角色。傷口癒合期間形成,新血管為受損皮膚提供氧氣和營養物質。新血管形成可以通過血管新生(指從無到有形成新血管或從現有血管形成新血管)發生。儘管許多種不同的介質可調節血管生成,其中VEGF是被認為是創傷癒合過程中最重要的促血管生成因子之一。
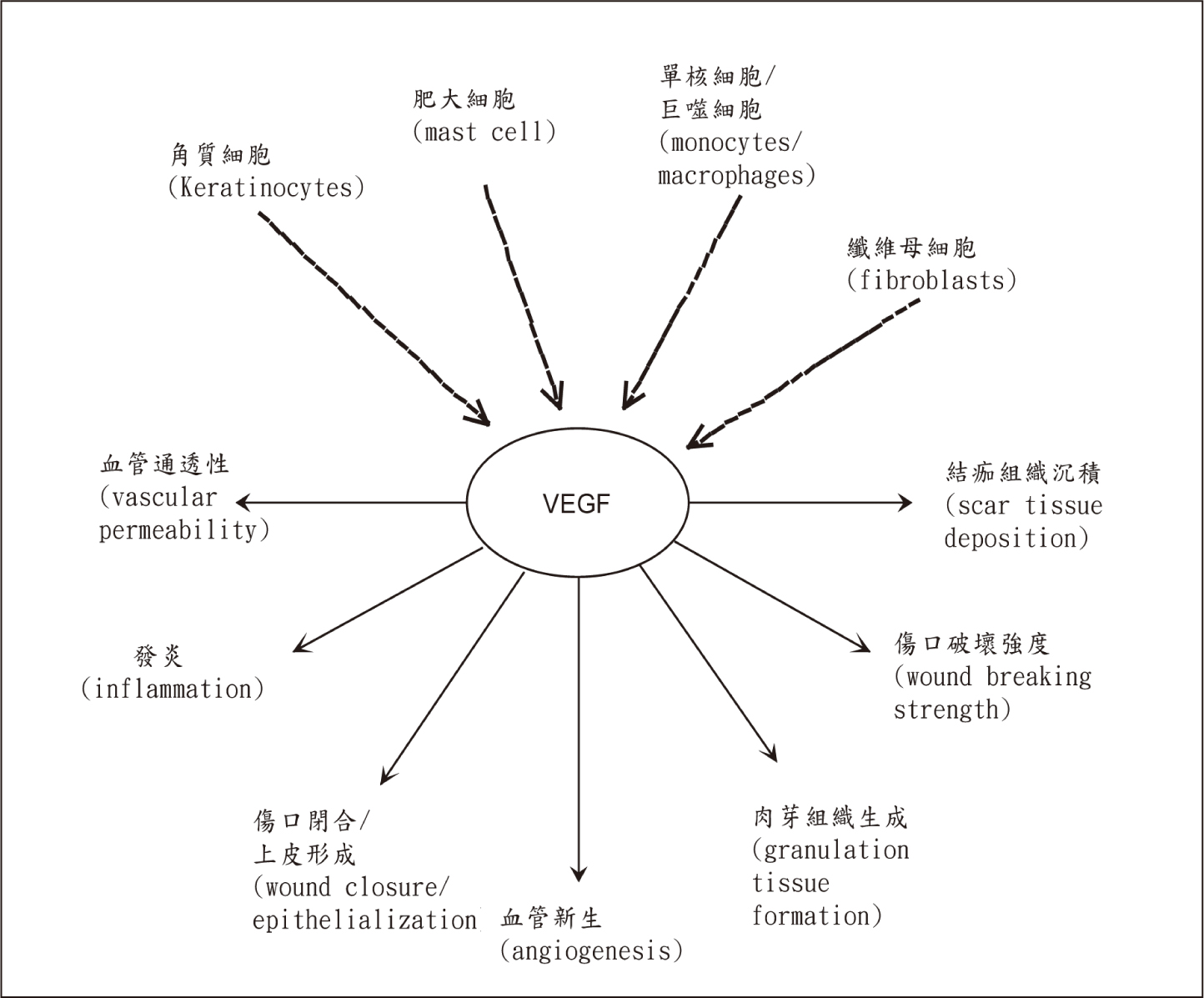
在修復傷口的過程中,有多種細胞與細胞損傷後的VEGF增加有關,包括角質細胞、巨噬細胞和纖維母細胞 (如圖一)。VEGF平常在表皮角質細胞以低濃度存在,但在受傷的傷口中增加濃度,而缺氧是傷口癒合過程中VEGF增加的原因之一,受傷皮膚中的低氧濃度活化轉錄因子,轉錄成VEGF基因,受傷產生的氧化劑,例如過氧化氫,以及在受傷部位產生的各種其他介質(包括表皮生長因子、角質生長因子、轉化生長因子和腫瘤壞死因子)也可以刺激角質細胞生成VEGF,進而促使血管生成反應。2
圖一 VEGF 在傷口癒合過程中細胞來源和作用
VEGF由多種細胞產生,包括角質細胞、肥大細胞、巨噬細胞和纖維母細胞(虛線箭頭)。而受傷後產生的VEGF會影響傷口癒合(實線箭頭)。
肆、藥物手術前須停藥時間
手術前停藥、手術後恢復藥物的時機和手術中的併發症相關。長期停用可降低併發症的發生率,但可能增加腫瘤再次惡化的風險。以下將一一介紹常見相關標靶藥物,分為針劑(bevacizumab和ramucirumab)和口服藥物(VEGF相關機轉有axitinib、lenvatinib、pazopanib HCl、sunitinib和sorafenib,哺乳類rapamycin標靶﹝mammalian target of rapamycin, mTOR﹞相關機轉有Everolimus)。
一、Bevacizumab (Avastin®)
Bevacizumab是一種重組的人化單株抗體,可選擇性地結合至VEGF並中和其生物活性。會抑制VEGF與位於內皮細胞表面上的受體fms Related Receptor Tyrosine Kinase 1(Flt-1)及kinase insert domain receptor (KDR)結合,中和VEGF的生物活性而降低腫瘤的血管形成,藉此抑制腫瘤的生長。
因為bevacizumab可能會對傷口癒合造成不利的影響,因此在第三期的臨床試驗中,排除過去28天內進行過重大手術的病人。在轉移性大腸直腸癌的臨床試驗中,患者在進行重大的手術後28到60天之間開始接受bevacizumab治療,其發生術後出血或傷口癒合併發症的危險性並未增加。故廠商建議在進行重大手術前,應暫停使用bevacizumab至少28天,在手術後至少28天且手術傷口完全癒合後再開始進行bevacizumab的治療。3
二、Ramucirumab (Cyramza®)
Ramucirumab是VEGFR 2拮抗劑,與VEGFR 2結合並阻斷其與VEGFR配體-VEGF-A、VEGF-C及VEGF-D的結合。因此ramucirumab能抑制配體刺激VEGFR 2活化,進而抑制配體誘發的增生活動及人類內皮細胞的移動。
在手術之前,ramucirumab應短暫停止使用至少4週。如果有傷口癒合的問題,ramucirumab應短暫停止使用,直到臨床上判斷傷口完全癒合,再開始使用。3
三、Axitinib (Inlyta®)
Axitinib是抑制酪胺酸激酶,包括VEGFR-1、VEGFR-2及VEGFR-3的作用。這些接受體都和病理性血管新生、腫瘤生長及癌症進展有關。
在進行排定的手術之前,應停止使用axitinib治療至少24小時。手術後重新開始使用的決定應以傷口是否充分癒合的臨床判斷做為依據。3
四、Lenvatinib (Lenvima®)
Lenvatinib是一種激酶抑制劑,會抑制VEGF受體 VEGFR1 (FLT1)、VEGFR2 (KDR)和VEGFR3 (FLT4)之激酶活性。
組織受損或手術中發現延遲傷口癒合的時間很廣(4-58天不等),應於進行定期手術6天前停用lenvatinib,相當於5次的lenvatinib半衰期(半衰期約28小時),並在術後基於對傷口能否充分癒合的臨床判斷再決定是否須要使用lenvatinib。4
五、Pazopanib HCl (Votrient®)
Pazopanib是一種多重酪胺酸酶抑制劑,作用目標和傷口癒合相關包括血管內皮生長因子受體VEGFR1-3。體內試驗則顯示,pazopanib 可抑制小鼠肺部內由VEGF 誘導的VEGFR-2 磷酸化、小鼠的血管新生,以及小鼠體內人類腫瘤異體移植的生長。
應於排定手術至少7天前停用 pazopanib。手術後應評估傷口癒合足夠,再考慮恢復 pazopanib使用。傷口裂開則應停用pazopanib。3
六、Sunitinib (Sutent®)
Sunitinib malate可抑制多種酪胺酸激酶接受體(Receptor Tyrosine Kinase, RTK),其中有些RTK與腫瘤生長、病理性血管新生、癌細胞轉移有關。評估sunitinib 對於多種激酶(超過80種激酶)的抑制活性後發現,和傷口癒合相關的機轉為血管內皮生長因子接受體(VEGFR1-3)。
Sunitinib應在手術時暫時停止用藥,sunitinib的半衰期為40小時,因此在外科手術之前停用sunitinib 1週或大約5個半衰期,使有足夠的時間防止干擾血管新生、止血和傷口癒合。5
七、Sorafenib (Nexavar®)
Sorafenib被證實可抑制多種細胞內(cellular homolog of viral raf gene、v-raf murine sarcoma viral oncogene homolog B1﹝BRAF﹞和突變型BRAF)及細胞表面激酶(和傷口癒合相關的為VEGFR1-3)反應。
2010回顧性研究指出,長期使用sorafenib可能嚴重延遲手術後傷口癒合並增加術後出血和血栓形成的風險。作者認為手術前停止藥物2或3個半衰期,可能會更安全,由於sorafenib的半衰期是1到2天,故停藥3或4天較安全。進行常規手術,例如部份或全腎臟切除手術,手術前停藥3天,若進行大手術,例如下腔靜脈血栓切除術或伴有腸道或鄰近器官轉移瘤切除術,建議手術前停藥7天,並在確認手術傷口癒合後至少7天再考慮恢復酪氨酸激酶抑制劑(Tyrosine kinase inhibitor,TKI)。6在一篇2015臨床研究中提出,有些人認為停藥和手術之間須要2週,這一篇研究是停藥7-16天再進行手術,除了一位患者有嚴重的腫瘤沾粘,其他不管是術中或術後都沒有副作用的發生,所有患者皆在手術的2週內出院。6
另一個2014年研究指出,手術前1-7天前停用sorafenib任何主要手術併發症或死亡率沒有增加。7在2008年另一較大的研究,探討手術前使用標靶藥物的安全性(其中44個患者中sorafenib有12位),sorafenib在手術前至少停藥1天,手術相關各項參數(包括手術中的死亡率、再次入院、血管栓塞、心血管、肺、胃腸道、感染和手術傷口併發症)和對照組沒有差異。8另一篇2014年進行研究指出若有手術或放射線治療,在肝癌和腎臟惡性腫瘤的患者有小於1%會發生囊腫,因擔心灌流減少使傷口癒合較差,故建議手術前24小時停藥,當傷口完全癒合後再開始使用藥物。另外有觀察到,有些因為緊急手術而沒有停止sorafenib,也沒有任何傷口癒合的問題。9
八、Regorafenib (Stivarga®)
Regorafenib是多種膜上激酶及細胞內激酶的小分子抑制劑,抑制和傷口癒合相關的機轉為VEGFR1-3,對致癌基因蘇氨酸激酶、酪氨酸激酶等標的有拮抗作用。
因有VEGF抑制劑會影響傷口的癒合,因此預定手術前2週必須停止使用regorafenib。手術後則根據臨床傷口癒合情形來判斷是否再次使用regorafenib。傷口裂開的病患須停止使用regorafenib。3
九、Everolimus (Afinitor®)
Everolimus為mTOR抑制劑,在 PI3K/AKT 路徑下游。Everolimus 會抑制缺氧誘導因子 (如 HIF-1轉錄因子) 的表現,及降低血管內皮生長因子 VEGF 表現。PI3K/Akt/mTOR 路徑的本質性活化會導致乳癌對荷爾蒙治療產生阻抗作用。
Everolimus (0.75 or 1.0 mg BID加上標準劑量或降低劑量的tacrolimus或 cyclosporine )的傷合癒合問題:包括任何傷口癒合事件發生率為11%-35%、 淋巴囊腫7%-16%、傷口裂開1.5%和切口露出3%,當患者接受高負荷劑量的mTOR抑制劑時,mTOR抑制劑相對於其他免疫抑制劑發生切口露出和淋巴囊腫的發生率更高。mTOR抑制劑阻斷內皮細胞和纖維細胞增生所需的生長信號,進而限制纖維化,抑制傷口癒合成功的關鍵因素,mTOR抑制劑還抑制VEGF和一氧化氮,它們是皮膚傷口中血管生成、發炎和免疫功能的調節劑。增加mTOR抑制劑相關傷口癒合風險的因素,包括年齡、糖尿病、營養不良、皮質類固醇、抗凝血劑使用、身高體重指數、抗胸腺免疫球蛋白誘導和長期手術時間。如果患者需要手術並且mTOR抑制劑治療可以安全地中斷,那麼可以在手術前至少1週停止mTOR抑制劑,治療並在10至15天後恢復mTOR抑制劑治療來減少傷口相關副作用的風險。10
2012年研究腎細胞癌標靶藥物的回顧性研究,3例(1%)患者有發生傷口癒合困難。因此,接受手術的患者中使用這些藥物需謹慎。然而,關於術前或術後治療中斷的最佳時間,並沒有明確的建議,作者建議mTORs應在手術前至少1週中斷,並在足夠的傷口癒合前不可使用,未來須定義選擇不同手術須停藥的最少時間。11
表 抗血管新生藥物的停藥時間3-6,8-11
伍、結論
越來越多的病人接受標靶藥物治療後延長了壽命,故現今的重點在如何管理相關的不良事件,而標靶藥物和傳統上細胞毒性藥物或免疫療法有很大不同。
由於此次搜尋文章,僅為評論性及研究性文章,研究性文章多為回溯性研究,所以仍缺乏大型研究的證實,未來仍須仰仗更嚴謹的隨機分派臨床試驗來研究與證實藥物和手術停藥相關時間,期望標靶藥物的使用能更有效及安全的用於癌症病人。
本文回顧標靶藥物增加手術傷口癒合風險,並列出常見相關藥品,使藥師在評估病人過去疾病史及藥物使用上扮演一個重要角色,依自身專業知識提供醫護人員藥品相關資訊,期能因藥師介入預防副作用及儘早介入以避免治療延遲。
Surgical Wound Healing Risks Associated with the Use of Targeted Drug Therapy
Chang-Chi Cheuh, Ming-Shyan Wang
Department of Pharmacy, Far Eastern Memorial
Hospital
Abstract
Wound healing complication is one of the side effects of targeted therapy. Vascular endothelial growth factor plays one of the most important pro-angiogenic factors in the mechanism of wound healing. Targeted therapy inhibits these vascular endothelial growth factors, thus impacting wound healing. At present, there is no comprehensive study about wounds healing complication caused by targeted therapy. This article will provide further understanding of the timing of drug withdrawal prior to surgery and drug resumption after surgery for clinical application.
參考資料:
1. P Martin, R Nunan: Cellular and molecular mechanisms of repair in acute and chronic wound healing. Br J Dermatol. 2015; 173(2): 370–8.
2. Kelly E Johnson, Traci A Wilgus: Vascular Endothelial Growth Factor and Angiogenesis in the Regulation of Cutaneous Wound Repair. 2014 ; 3(10): 647–61.
3. Bevacizumab (Avastin®)癌思停注射劑中文仿單,Ramucirumab (Cyramza®)欣銳擇注射劑中文仿單,Axitinib (Inlyta®)抑癌特膜衣錠中文仿單,Pazopanib HCl (Votrient®)福退癌膜衣錠中文仿單,Regorafenib (Stivarga®)癌瑞格膜衣錠中文仿單
4. Connie Cheng, Afrouz Nayernama, S Christopher Jones, et al: Wound healing complications with lenvatinib identified in a pharmacovigilance database. J Oncol Pharm Pract . 2019;25(8):1817-22.
5. Anita Schwandt, Laura S Wood, Brian Rini, et al: Management of side effects associated with sunitinib therapy for patients with renal cell carcinoma.Onco Targets Ther. 2009; 2: 51–61.
6. Tsunenori Kondo, Yasunobu Hashimoto, Hirohito Kobayashi, et al: Presurgical Targeted Therapy with Tyrosine Kinase Inhibitors for Advanced Renal Cell Carcinoma: Clinical Results and Histopathological Therapeutic Effects. Jpn J Clin Oncol. 2010;40(12):1173-9.
7. Vijaya R Bhatt , Apar Kishor Ganti, James K Schwarz, et al: Safety and efficacy of preoperative sorafenib therapy in facilitating cytoreductive surgery in renal cell carcinoma.Future Oncol. 2014;10(5):703-6.
8. Vitaly Margulis, Surena F Matin, Nizar Tannir, et al: Surgical Morbidity Associated With Administration of Targeted Molecular Therapies Before Cytoreductive Nephrectomy or Resection of Locally Recurrent Renal Cell Carcinoma. J Urol. 2008 ;180(1):94-8.
9. Marcia S Brose, Catherine T Frenette, Stephen M Keefe, et al: Management of sorafenib-related adverse events: a clinician's perspective. Semin Oncol. 2014;41(2):S1-S16.10. Bruce Kaplan, Yasir Qazi, , Jason R Wellen: Strategies for the management of adverse events associated with mTOR inhibitors.Transplant Rev (Orlando). 2014 ;28(3):126-33.
10. Tim Eisen, Cora N Sternberg, Caroline Robert, et al: Targeted therapies for renal cell carcinoma: review of adverse event management strategies. J Natl Cancer Inst. 2012 ;104(2):93-113.
通訊作者:闕昌琪/通訊地址:新北市板橋區南雅南路二段21號藥學部
服務單位:亞東紀念醫院藥學部/聯絡電話:(O) 02-89667000 ext 1115